Сравните по следующим параметрам серу и кремний: а) количество элементарных частиц
б) заряд ядра
в) количество электронных слоёв
г) радиус атома
д) число электронов на внешнем слое
Ответы на вопрос:
7994 грамма
Объяснение:
Известен тип реакции(обмена) основания и ангидрида:
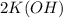 +
+ 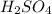 =
= 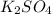 +
+ 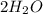
Если раствор сульфата калия и воды это 100% то вычитая из массы раствора массу серной кислоты можно получить процент содержания основания в реагентах.
Вычислить процент серной кислоты в составе реагентов так как по закону сохранения масс веществ реакция не меняет числовые значения содержания атомов элементов в растворе.
Процент вещества в составе смеси реагентов вычисляется сравнения относительной молекулярной массы нужного соединения с суммой масс веществ всего раствора:
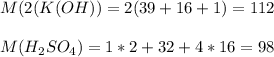
112+98 = 210 дальтон => 98:210*100 = 46,(6) % - процент массы кислоты
значит процент основания от общей массы 53.4%
Процент воды в растворе продуктов 21%
21/79 = 0.26 => 0.26* 13552 = 3602.4 г -масса воды в растворе
13552 + 3602.4 = 17154,4г масса всего раствора продуктов
53.4 / 100 * 17154.4г = 9160,4 г - масса серной кислоты в реагентах
Следовательно:
17154.4г - 9160,4 = 7994 грамма гидроксида калия было израсходовано
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
3 вопрос Лайк и оценка...
 nadjanikiforovp0bx4027.04.2021 10:42
nadjanikiforovp0bx4027.04.2021 10:42 -
Составьте уравнения реакций следующих превращений: Pb(NO3)2 →Pb(OH)2...
 АмерикаСингер85231.01.2022 12:37
АмерикаСингер85231.01.2022 12:37 -
Нужна ! Обчисліть масову частку натрій гідроксиду в розчині масою...
 Дахич121.03.2022 19:35
Дахич121.03.2022 19:35 -
Визначити формулу сполуки з масовою часткою карбону 80%з гідрогеном...
 Iskrmsndrxjdjjsd28.07.2022 15:32
Iskrmsndrxjdjjsd28.07.2022 15:32 -
1.в ставку 3000*1023 молекул води. Обчисліть масу та о бєм води в...
 belkairi07.06.2021 15:08
belkairi07.06.2021 15:08 -
к 1 л 50% - ого раствора азотной кислоты (p=1310г/см3) добавили 690...
 Yulia1492909.06.2021 23:21
Yulia1492909.06.2021 23:21 -
Сравнительная характеристика галогенов и халькогенов! прошу...
 poliaprokopets21.05.2023 11:45
poliaprokopets21.05.2023 11:45 -
Сколько хлора выделится при реакции 36.5%ного хлорида кислоты массой...
 skosachyov01.07.2020 08:41
skosachyov01.07.2020 08:41 -
Четырехэлементарые вещества: 1)анилин 2)глицин 3)мочевина 4)карболовая...
 annapetrovakons14.09.2022 12:41
annapetrovakons14.09.2022 12:41 -
Сколько аллотропных видоизменений имеет сера...
 mklslajh06.06.2021 01:54
mklslajh06.06.2021 01:54

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
