При взаимодействии 2г. смеси порошков железа и магния с избытком соляной кислоты, выделилось 0.05моль водорода. определите массовый состав смеси в %.
217
385
Ответы на вопрос:
Fe + 2hcl = fecl2 + h2 mg + 2hcl - mgcl2 + h2 пусть х моль - n(fe), у моль - n(mg) тогда: m(fe) = 56х г, m(mg) = 24у составим уравнение: 56х + 24у = 2 по уравнению реакции: n(h2) = n(fe) = х моль n(h2) = n(mg) = y моль составим уравнение: х + у = 0,05 составим систему: 56х + 24у = 2г х + у = 0,05 домножим второе уравнение на 24: 56х + 24у = 2 24х + 24у = 1,2 вычтем из 1 уравнения второе: 32х = 0,8 х = 0,025 н = 0,05-0,025 = 0,025моль m(fe) = 0,025моль*56г/моль = 1,4г w(fe) = m(fe)/m(смеси)*100% = 1,4г/2г*100% = 70% w(mg) = 100% - 70% = 30%
7)
Оксид Ag,оксид Cr(III),оксид С(II),оксид Cl(VII),оксид N(II),оксид N(IV),оксид Si(II),оксид Fe(III),оксид P(III),оксид Sr(II),оксид Sb(V),оксид Mn(VII),оксид S(IV)
Оксиды металлов:1,2,8,10
8) фото
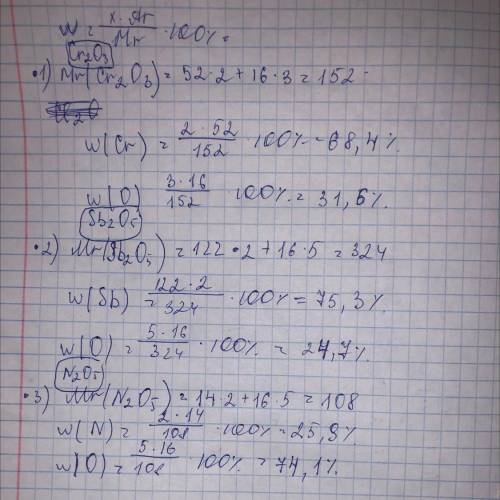
Оксид Ag,оксид Cr(III),оксид С(II),оксид Cl(VII),оксид N(II),оксид N(IV),оксид Si(II),оксид Fe(III),оксид P(III),оксид Sr(II),оксид Sb(V),оксид Mn(VII),оксид S(IV)
Оксиды металлов:1,2,8,10
8) фото
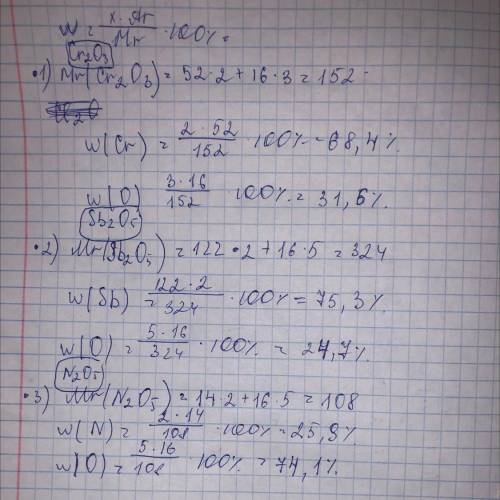
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Осуществить цепочку превращений...
 урааа2815.03.2021 23:43
урааа2815.03.2021 23:43 -
Сколько грамм сульфат железа образуется при взаимодействии хлорида железа 80...
 verakong04.01.2021 19:37
verakong04.01.2021 19:37 -
Как изменится массовая доля (в%) соли в растворе, если к 0,24 кг 10-процентного...
 COYOT6124.02.2021 14:12
COYOT6124.02.2021 14:12 -
Дайтее ответыыыыыыыы нужноооооооооо ...
 heybibl21104.04.2023 19:33
heybibl21104.04.2023 19:33 -
6. зв’язок між кількістю речовини й масою описується формулою: 7. обчисліть кількість...
 Соня1164712.07.2020 09:49
Соня1164712.07.2020 09:49 -
Яне понимаю формулу 2n во второй степени, обьясните кому не сложно...
 Masha827128.05.2023 17:33
Masha827128.05.2023 17:33 -
Поместите в пробирку немного черного порошка меди,прилейте в нее 1-2 мл раствора...
 laykutina09.01.2023 09:12
laykutina09.01.2023 09:12 -
Какие два вида связи могут одновременно встречаться в молекулах каких-либо соединений...
 Dodgesantafe17.11.2021 01:07
Dodgesantafe17.11.2021 01:07 -
Какую массу 10 %-ого расствора можно приготовить из 50 г h2so4?...
 Вишенка01112.04.2023 20:50
Вишенка01112.04.2023 20:50 -
1.из ниже перечня формул выпишите в два столбика формулы оксидов металлов и оксидов...
 azolin5674567424.07.2021 16:17
azolin5674567424.07.2021 16:17

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
