Необходимо приготовить сплав олова со свинцом, в котором массовая доля свинца 46,5% какую массу оксида олова4 и оксида свинца2 надо взять чтобы при восстановлении их углем получился сплав массой 44,5г
250
303
Ответы на вопрос:
1. найдем массовую долю олова в сплаве: w(sn)=100%-46,5%=53,5%2. вычислим массу каждого металла в сплаве: m(pb)=89 г*0,465=41,385 гm(sn)=89 г*0,535=47,615 г3. составим уравнение реакции восстановления оксида свинца(2) углём: pbo + c = pb + co4. вычислим количество вещества - свинца (pb) по формуле n=m\mn(pb)=41,385г\ 207 г\моль≈0,2 моль5. по уравнению реакции найдём количество вещества - оксида свинца(2) -pbo ( сравним коэффициенты : перед свинцом и оксидом свинца(2) стоит коэффициент 1 , так как 1=1, то n(pb)=n(pbo): по уравнению реакции: n(pbo)=n(pb)=0,2 моль6. вычислим массу оксида свинца(2) по формуле m=n*m: m(pbo)=0,2 моль * 223 г\моль=44,6г7. составим уравнение восстановления углём оксида олова(4): sno₂ + c = sn + co₂ 8. найдём количество вещества олова(sn) по формуле n=m\m: n(sn) = 47,615г \ 119 г\моль=0,4 моль9. по уравнению реакции найдём количество вещества - оксида олова(4) - sno₂ ( сравним коэффициенты : перед оловом и оксидом олова(4) коэффициент равен 1, так как 1=1 , то n(sno₂)=n(sn): по уравнению реакции: n(sno₂ )=n(sn)=0,4 моль10. найдём массу оксида свинца(4)-sno₂ по формуле m=n*m m(sno₂ )=0,4 моль * 151 г\моль= 60,4г
Объяснение:
Начнем с того, что Al(OH)3 - не диссоциирует на ионы
Kд = 1,38 · 10-9 - константа диссоциации его
Kд = 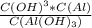 Если ты посмотришь на это уравнение, то заметишь что на миллиард гидроксидов распадется 1 ион алюминия(Al3+) и 3 иона OH-
Если ты посмотришь на это уравнение, то заметишь что на миллиард гидроксидов распадется 1 ион алюминия(Al3+) и 3 иона OH-
Т.е. фактически диссоциация не происходит
У нерастворимых соединений диссоциация не происходит
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Какой цвет имеет йод, выпавший в осадок?...
 shamil2004202.06.2022 14:34
shamil2004202.06.2022 14:34 -
При взаимодействии 300 г известняка с раствором азотной кислоты, выделилось...
 14862522.04.2023 08:37
14862522.04.2023 08:37 -
Название вещества: ch3-ch(ch3)-ch2-c(h)=0...
 mrkrbnv20.06.2021 09:56
mrkrbnv20.06.2021 09:56 -
Врезультате реакции оксида меди (||) с серной кислотой образовалось 40 г сульфата...
 VeronicaOgne15.03.2021 04:20
VeronicaOgne15.03.2021 04:20 -
Определите количество молекул 3г кислорода...
 anninor5314.02.2022 14:30
anninor5314.02.2022 14:30 -
6)В предложенном перечне отметьте название электролита, при диссоциации которого...
 kmelashenko15.07.2021 02:42
kmelashenko15.07.2021 02:42 -
1. Как называется заболевание, связанное с чрезмерным избытком витаминов в...
 12345644508.02.2023 06:31
12345644508.02.2023 06:31 -
17) Егор и Инна опытным путём выявили, что в пробирке № 1 присутствуют сульфат-ион...
 Amalik030.11.2022 03:35
Amalik030.11.2022 03:35 -
Как записать уравнение реакции с индикаторами? К примеру, Ca(OH)+индикаторная...
 БезликийNoName26.04.2020 22:24
БезликийNoName26.04.2020 22:24 -
Массовая доля соли в насыщенном растворе при некоторой температуре равна 28,...
 wasyr13415.10.2020 08:51
wasyr13415.10.2020 08:51

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
