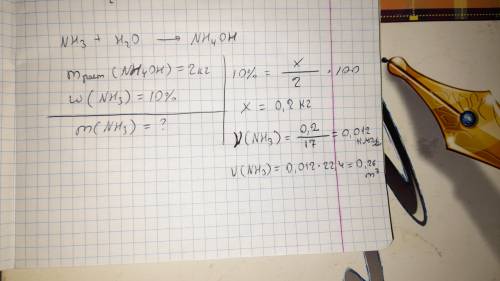3-39. Для обеззараживания используют 10%-ый раствор нашатырного спирта NH4OH. Вычислите, какой объём аммиака NH3 нужно растворить в воде для получения 2кг раствора
186
290
Ответы на вопрос:
1) 2ki + br2 = i2 + 2kbr
находим количество вещества йода. по уравнению реакции:
n(i2) = 2n(ki)
n(i2) = 0,4/2 = 0,2моль
вычисляем массу йода:
m(i2) = n x m = 0,2моль х 254г/моль = 50,8г
2)
а)feci2+k2cr2o7+hci → feci3+crci3+kci+h2o
2сr(+6) +6e = 2cr(+3) |1 окислитель (процесс - восстановление)
fe(+2) - 1e = fe(+3) | 6 восстановитель (процесс - окисление)
6feci2+k2cr2o7+14hci → 6feci3+2crci3+2kci+7h2o
b)nai+kmno4+koh → i2+k2mno4+naoh
- 2e = i2(0) |1 восстановитель (окисление)
mn(+7) + 1e = mn(+6) |2 окислитель (восстановление)
2nai+2kmno4+2koh → i2+2k2mno4+2naoh
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
A.Запишите, как изменяются свойства элементов 2-го и 3-го периодов...
 alina192223.08.2022 18:18
alina192223.08.2022 18:18 -
Олово 1.Охарактеризуйте металл, соответствующий номеру вашего варианта...
 07777108602.09.2021 10:39
07777108602.09.2021 10:39 -
В результате химической реакции между избытком раствора гидроксида...
 45r77yf21.05.2023 05:05
45r77yf21.05.2023 05:05 -
Составьте уравнения реакций, которые соответствуют превращениям:...
 VadimOMG25.01.2020 21:09
VadimOMG25.01.2020 21:09 -
Вещество между молекулами которого существует водородная связь а)ацетилен...
 Azizo44kka21.01.2023 21:55
Azizo44kka21.01.2023 21:55 -
Названия соединения : hno2, p2o5, ba(oh)2, k2so4, h2so4. напишите...
 3aHo3a153822.09.2020 16:00
3aHo3a153822.09.2020 16:00 -
Скакими из веществ будет взаимодействовать оксид кальция: hno3, koh,...
 anast20039702.02.2023 15:08
anast20039702.02.2023 15:08 -
Составте формулы соединений а) оксид натрия б)серноя кислота в) сульфад...
 lsofa120418.04.2022 07:32
lsofa120418.04.2022 07:32 -
Какой объем водорода выделится (н.у.) при взаимодействии избытка...
 Anna45w45628.06.2022 14:43
Anna45w45628.06.2022 14:43 -
1. вычислите количество и массу оксида кальция,образующегося при...
 sanya320215.04.2020 07:07
sanya320215.04.2020 07:07

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.