Здравствуйте , с химией, никак не пойму При сжигании неизвестного углеводорода массой 4.3 грамм образовалось 6.3 грамм воды и углекислый газ. Определите молекулярную формулу углеводорода и его структуру, если известно, что его молекула содержит два третичных атома углерода
Ответы на вопрос:
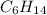
Диизопропил
2,3-диметилбутан
Объяснение:
Сейчас начнем решать это, просто примите как аксиому, что числа x и y, что мы найдем МОЖНО пропорционально увеличивать, то есть умножить или разделить на какое-то число, к примеру, если  , то
, то 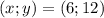 тоже будет верным, однако ответ все же конкретный, мы с вами воспользуемся этим в решении, перейдем к нему:
тоже будет верным, однако ответ все же конкретный, мы с вами воспользуемся этим в решении, перейдем к нему:
Нам не известен класс сгораемого вещества, запишем общую формулу горения углеводородов:
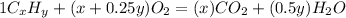
Вы сами можете прекрасно вывести эту формулу
Пусть мы имеем y атомов водорода, тогда согласно формуле, в воде у нас будет 0.5y атомов кислорода, запишем молярную массу воды

Из стехиометрического закона отношение коэффициентов перед веществами равно отношению количеств веществ, применим закон к CxHy и H2O
По тому же принципу, что и раньше молярная масса CxHy равняется 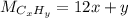
Количество вещества равняется масса (даны по условию) делить на молярную массу (для воды знаем, для углеводорода нашли)
Запишем закон:

Решив уравнение получим, что 
Напоминаю что числа x, y всего лишь коэффициенты, и их можно домножить
Домножим на знаменатель нецелой дроби, чтобы получить целые числа

Теперь, получив целые числа мы можем сказать, что формула вещества 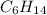 , выполним проверку, подставив значения:
, выполним проверку, подставив значения:
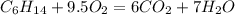
Если домножить на два, то получим классическое уравнение с целыми коэффициентами:

По закону стехиометрии проверяется что при сгорании 4.3 грамм вещества ДЕЙСТВИТЕЛЬНО образуется 6.3 грамма воды
Найдем структурную формулу:
Два атома соединены с тремя атомами углерода, выполнить это можно единственной конфигурацией, разместив в цепочке из 4 атомов углерода два метила к 2 и 3 атомам углерода, и получив диизопропил или 2,3-диметилбутан

Вещество состава C₆H₁₄ - 2,3-диметилбутан.
Объяснение:
Исходя из условия считаем, что углеводород состоит только из атомов углерода и водорода, в противном случае в условии задачи недостаточно данных.
Известно, что выделилось 6,3 г воды.
Молярная масса воды:
M(H₂O) = 2 + 16 = 18 г/моль.
Найдем количество вещества выделившейся воды:

Согласно формуле 1 моль воды содержит 2 моль атомов водорода.
Тогда 0,35 моль воды содержит 0,7 моль водорода, и столько же моль водорода содержит углеводород.
Масса атомов водорода m(H) = 0,7 моль · 1 г/моль = 0,7 грамм.
Тогда исходный углеводород содержит 0,7 г водорода и
4,3 г - 0,7 г = 3,6 г углерода.
Тогда отношение числа молей атомов углерода и водорода в исходном углеводороде:
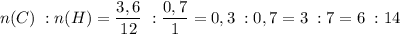
При n(С) = 3 имеем структуру состава C₃H₇- это радикал, пропил, часть молекулы с одной свободной связью.
при n(С) = 6 состав вещества C₆H₁₄, что соответствует составу предельных углеводородов CₙH₂ₙ₊₂.
Исходное вещество является изомером гексана, так как по условию его молекула содержит два третичных атома углерода.
2,3-диметилбутан.

Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Определите массу и объем углекислого газа, образовавшегося при сжигании...
 miroslav123412.02.2021 11:02
miroslav123412.02.2021 11:02 -
Найдите массу одного атома водорода и одной молекулы водорода....
 lizismik1507.09.2020 10:20
lizismik1507.09.2020 10:20 -
Найдите в Периодической системе химических элементов Д.И.Менделеева...
 Милкович1113.12.2021 16:00
Милкович1113.12.2021 16:00 -
Выберите пары веществ, между которыми возможно взаимодействие: гидроксид...
 Arinka2605200501.07.2022 06:51
Arinka2605200501.07.2022 06:51 -
Определите объём газа(н.у.), выделившегося при взаимодействии питьевой...
 ВиГуки24716.09.2022 11:57
ВиГуки24716.09.2022 11:57 -
Имеется смесь оксидов Al2O3 и Feo при обработке которой избытком...
 adeka08827.02.2021 07:28
adeka08827.02.2021 07:28 -
Вступает ли этиловый спирт в реакцию с карбонатом натрия? Если да,...
 grenika29.11.2021 19:51
grenika29.11.2021 19:51 -
Выбери верные утверждения: свойства органических веществ зависят...
 боб6808.06.2022 11:50
боб6808.06.2022 11:50 -
20 балов Олеиновая кислота не реагирует с: Na2O C6H12 C3H7OH Cl2...
 Znatokiys12.03.2020 20:31
Znatokiys12.03.2020 20:31 -
мне посоветуйте что надо делать...
 yusifmailov101.05.2020 09:31
yusifmailov101.05.2020 09:31

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
