, решить! Смесь цинка и магния массой 8,9 г растворили в избытке соляной кислоты. В результате реакции выделилось 4,48 л (н.у.) водорода. Рассчитайте массовую долю (%, до целых) цинка в смеси.
Ответы на вопрос:
Массовая доля цинка равна 73.03 %
Объяснение:
Дано:
m(смеси)=8.9 г
V(H2)=4.48 л
Найти
w(Zn)-?
m(смеси)=m(Zn)+m(Mg)=8.9
Zn+2HCl=ZnCl2+H2
Mg+2HCl=MgCl2+H2
M(Mg)=24 г/моль
M(Zn)=65 г/моль
n(Zn)=n(H2)
n(Mg)=n(H2)
n(H2)=V/Vm=4.48/22.4=0.2 моль
n(Zn)*M(Zn)+n(Mg)*M(Mg)=8.9
n(Zn)+n(Mg)=0.2 моль
n(Zn)*M(Zn)+(0.2-n(Zn))*M(Mg)=8.9
n(Zn)*65+0.2*24-n(Zn)*24=8.9
n(Zn)*(65-24)=4.1
n(Zn)=0.1 моль
m(Zn)=0.1*65=6.5 г
w(Zn)=6.5/8.9=0.7303 м.д.=73.03 %
Дано:
m(смеси) = 8,9 гр
V(H₂) = 4,48 л
Найти:
ω(Zn) - ?
1) Для начала мы запишем уравнений реакций то что известно по условию задачи:
Zn + 2HCl(изб.) → ZnCl₂ + H₂↑ (1)
Mg + 2HCl(изб.) → MgCl₂ + H₂↑ (2)
2) Далее находим количества вещества у водорода:
Vm = 22,4 л/моль
n(H₂) = V(H₂)/Vm = 4,48 л / 22,4 л/моль = 0,2 моль
3) Теперь находим количества веществ у цинка и у меди, а потом водорода по их реакциям:
Пусть m(Zn) = x гр, тогда m(Mg) = (8,9 - x) гр, следовательно:
M(Zn) = 65 гр/моль M(Mg) = 24 гр/моль
n(Zn) = m(Zn)/M(Zn) = x гр / 65 гр/моль = x/65 моль ⇒ n₁(H₂) = n(Zn) = x/65 моль - из (1) уравнений реакций
n(Mg) = m(Mg)/M(Mg) = (8,9 - x) гр / 24 гр/моль = (8,9 - x)/24 моль ⇒ n₂(H₂) = n(Mg) = (8,9 - x)/24 моль - из (2) уравнений реакций
4) Теперь решаем уравнение:
n₁(H₂) + n₂(H₂) = n(H₂)
x/65 + (8,9 - x)/24 = 0,2 моль | × 1560
24x + 65(8,9 - x) = 312
24x + 578,5 - 65x = 312
24x - 65x = 312 - 578,5
-41x = -266,5 | : (-41)
x = 6,5 гр ⇒ m(Zn) = 6,5 гр
5) Теперь находим массовую долю цинка:
ω(Zn) = m(Zn)/m(смеси) × 100% = 6,5 гр / 8,9 гр × 100% ≈ 0,73 × 100% ≈ 73%
ответ: ω(Zn) = 73%
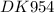
1) общая формула кристаллогидрата натрия сульфата:
na₂so₄* nh₂o
2) возьмем 1 моль данного кристаллогидрата, сульфур в 1 моле имеет массу 32 г и составляет 9,94%. на основании этого составляем пропорции и находим процентное содержание остальных элементов.
32 г сульфура составляет 9,94%
46 г натрия х%
х = 46*9,94/32 = 14,28875% - это процентное содержание натрия
32 г сульфура составляет 9,94%
64 г оксигена х%
х = 64*9,94/32 = 19,88 - это процентное содержание оксигена.
3) итого процентное содержание сульфата натрия в его кристаллогидрате равно: 9,94 + 14,28875 + 19,88 = 14,10875%
4) тогда процентное содержание воды в кристаллогидрате равно:
100 - 14,10875 = 55,89125%
5) находим массу воды в 1 моле кристаллогидрата:
32 г сульфура составляет 9,94%
х г воды 55,89125%
х = 32*55,89125/9,94 ≈ 180 г
масса 1 моля воды 18 г/моль, значит число молей воды равно:
180/18 = 10 моль
значит формула кристаллогидрата: na₂so₄* 10h₂o
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Определите массовую долю naoh? если 40 г его расстворили в 160 г воды...
 shukirbekovabak19.06.2023 02:26
shukirbekovabak19.06.2023 02:26 -
Какие массы соли и воды потребуется для приготовления 500г ее 15%-го раствора...
 Sanek27rus16.01.2020 22:49
Sanek27rus16.01.2020 22:49 -
Задача по химии В смеси находится 1 моль водорода, 1.5 моль аргона и 0.5 моль...
 MaykTV2623.05.2020 18:21
MaykTV2623.05.2020 18:21 -
Дано: Ню ( H3PO4)=33 моль Mr-? m-? N-? V-?...
 andreybalashov03.05.2021 23:06
andreybalashov03.05.2021 23:06 -
SO3 ➡️ MgSO4 ➡️ BaSO4 ⬇️ Mg(OH) 2...
 hedaku27.05.2022 22:25
hedaku27.05.2022 22:25 -
1. Наведи не менше п яти прикладів речовин, які є провідниками....
 manyna425.08.2020 13:43
manyna425.08.2020 13:43 -
Напишiть рiвняння реакцiй, за до яких можна здiйснити такi перетворення: Ba...
 Tiktak22224.12.2020 00:26
Tiktak22224.12.2020 00:26 -
Составьте структурную формулу 3 изомеров вещества состава C6 h14...
 hromgugd24.10.2020 11:12
hromgugd24.10.2020 11:12 -
Установите соответствие между формулой вещества и общей формулой гомологического...
 mariaK91812.05.2022 12:59
mariaK91812.05.2022 12:59 -
К классу алканов относится углеводород, формула которого: 1) C3H6 2) C3H4 3)...
 Джахаршин819.05.2020 09:37
Джахаршин819.05.2020 09:37

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
