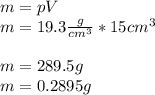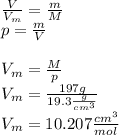. 1. Рассчитайте массу 15 см3 золота, если плотность золота равна 19,3 г/см3.
2. Рассчитайте молярный объём золота, если плотность золота равна 19,3 г/см3.
246
440
Ответы на вопрос:
1 — 289.5
2 — 10.2
Объяснение:
1. Чтобы найти массу вещества, объем надо умножить на плотность.
М=р*V
2. Чтобы найти молярный объем, нужно разделить молярную массу вещества на его плотность.
Vm=M/p
Для начала найдем массу nacl по формуле m = p * v mр-ра(nacl) = 1,086 г/мл * 120 мл = 130,2 г mр.в. (nacl) = 130,2г * 0,12 = 15,624г теперь найдем кол-во вещества и определим, где избыток, а где недостаток, чтобы потом найти массу agcl n (nacl) = m\m = 15,624г : 58,5г/моль = 0,27 моль (избыток) точно так же находим массу и ню agno3 mр-ра(agno3) = 1,05 г/мл * 100 мл = 105 г mр.в.(agno3) = 105г * 0,06 = 6,3 г n (agno3) = 6,3г : 170 г/моль = 0,037 моль ( недостаток) смотрим по недостатку n(agno3) = n (agcl) = 0,037 моль m(agcl) = m*n =143,5 г/моль * 0,037 моль = 5,3 г ответ: 5,3 г
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Сколько граммов соли необходимо растворить в 340 мл воды, чтобы получить 15%-ный...
 sadyk77103.04.2023 18:15
sadyk77103.04.2023 18:15 -
Какова масса 0.5 моль нитрата серебра(agno3)?...
 allihen17.07.2020 00:53
allihen17.07.2020 00:53 -
Напишите строение и состав моносахаридов...
 Болус24.02.2022 23:01
Болус24.02.2022 23:01 -
Запишите уравнения возможных реакций...
 KekLol8905.04.2020 16:28
KekLol8905.04.2020 16:28 -
Доказать с уравнения реакций характер оксидов n2o3,b2o,cr2o3. и гидроксидов...
 bondarsvetlana2520.03.2023 22:34
bondarsvetlana2520.03.2023 22:34 -
ТЕ 4. Дописати рівняння реакцій і вказати, з якої причини відбуваться кожна...
 Саша1281124.08.2022 21:32
Саша1281124.08.2022 21:32 -
Допишіть схеми реакцій і Перетворіть їх на хімічні рівняння для рівняння б...
 Five1103.05.2021 20:43
Five1103.05.2021 20:43 -
Дуже треба напишіть рівняння хімічних реакцій, за якими можна здійснити хімічні...
 yanaboss66615.08.2021 18:18
yanaboss66615.08.2021 18:18 -
До ть виконати.Обчисліть масові частки Карбону і Гідрогену у октані? ів...
 генадийпетрович02.05.2023 19:28
генадийпетрович02.05.2023 19:28 -
Складіть рівняння реакцій для здійснення ланцюга перетворень. Дайте назви...
 юля273828.05.2020 11:34
юля273828.05.2020 11:34

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.