Какая реакция относится к реакциям обмена: а) al2o3+hcl→, б) na2o + h2o→, в) fe + h2so4 →, г) caco3 → .какая реакция относится к реакциям соединения: а) al2o3+hcl→, б) na2o + h2o→, в) fe + h2so4 →, г) caco3 →. какое уравнение соответствует реакции разложения: 1) zn+cuso4=znso4+cu 2)bacl2+k2co3=baco3+2kcl, 3) cao+co2+caco3, 4) fe(oh)2=feo+h2o. какое уравнение соответствует реакции замещения: 1) co2+h2)=h2co3, 2) c+2h2=ch4, 3) 2h2o=2h2+o2, 4) 2 h2o+2na=2naoh+h2 наиболее энергично реагирует с водой: а) калий, б) кальций, в) скандий, г) магний. какой из указанных металлов проявляет наибольшую активность в реакции с соляной кислотой: 1) свинец, 2) магний, 3) цинк, 4) медь. определите коэффициент перед простым веществом в уравнении: al + h2so4 = al2(so4)3 + h2oа) 1, б) 2, в) 3, г) 4
136
210
Ответы на вопрос:
какая реакция относится к реакциям обмена:
а) al₂o₃+hcl→
какая реакция относится к реакциям соединения:
б) na₂o + h₂o→
какое уравнение соответствует реакции разложения:
4) fe(oh)₂=feo+h₂o
какое уравнение соответствует реакции замещения:
4) 2h₂o+2na=2naoh+h₂
наиболее энергично реагирует с водой: а) калий
какой из указанных металлов проявляет наибольшую активность в реакции с соляной кислотой: 3) цинк
определите коэффициент перед простым веществом в уравнении: б) 2
Примеры 3 основных кислот см в разделе "Объяснение".
Объяснение:
1) Серная кислота.
Формула: 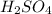 ;
;
Кислотный остаток: Сульфит.
2) Азотная кислота.
Формула: 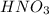 ;
;
Кислотный остаток: Нитрат.
3) Угольная кислота.
Формула: 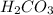 ;
;
Кислотный остаток: Карбонат.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Одним из способов получения серы является обжиг fes_2. дайте название этого...
 lao120525.06.2023 14:30
lao120525.06.2023 14:30 -
Взакрытом реакторе взорвали смесь равных объемов водорода и кислорода....
 mmatomagomedova22.08.2021 04:37
mmatomagomedova22.08.2021 04:37 -
Кількість речовини води, у якій міститься таке ж число атомів, що і в кисні...
 freax161301.02.2020 20:27
freax161301.02.2020 20:27 -
На титрование 40 мл раствора серной кислоты затрачено 15 мл 0,1000 раствора...
 hedaku03.03.2022 21:18
hedaku03.03.2022 21:18 -
Какое количество соли образуется при взаимодействии 20 г карбоната натрия...
 viktoriasmirnova20025.03.2020 11:27
viktoriasmirnova20025.03.2020 11:27 -
Нужно решить для допуска к экзаменам. рассчитать эдс цепи образованной...
 gvg197111.10.2021 07:54
gvg197111.10.2021 07:54 -
Сожгли 7,8г к. определить объем o2израсходоного при этом. ...
 Mika12312309.05.2023 12:36
Mika12312309.05.2023 12:36 -
Обчисліть масу етилетаноату,що можна добути зі 100 г оцтової есенції,яка...
 cvacvadav03.05.2023 22:36
cvacvadav03.05.2023 22:36 -
Уровнять методом электронного баланса: H2SO4= CO2+SO2+H2O...
 kravchenko171201.11.2020 10:58
kravchenko171201.11.2020 10:58 -
По ухр so2 +o2→so3 вычислите, какой объем кислорода необходим для окисления...
 Alinыch1109.06.2021 12:57
Alinыch1109.06.2021 12:57

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
