Какой объем газа образуется при взаимодействии 12 г магния,содержащего 10% примесей соляной кислоты?
Ответы на вопрос:
Масса образовавшегося йода 50,8 г.
Объяснение:
Через раствор, содержащий 60 г иодида натрия, пропустили хлор объемом 15,6 л (н.у.). Определите массу образовавшегося йода.
Дано:
m(NaI) = 60 г;
V(Cl₂) = 15,6 л.
Найти: m(I₂).
Решение.
Более сильные галогены вытесняют более слабые из солей. Хлор вытесняет йод из солей.1) Запишем уравнения реакции между иодидом натрия и хлором, в результате которой образуется йод и хлорид натрия.
2NaI + Cl₂ → I₂ + 2NaCl
2) Найдем количество вещества иодида натрия, взятого для реакции.
M(NaCl) = 23 + 127 =150 г/моль.
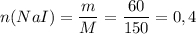 (моль)
(моль)
4) Найдем количество вещества хлора.
По закону Авогадро 1 моль любого газа занимает объем 22,4 л.
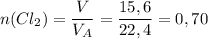 (моль).
(моль).
5) Определим количество выделившегося йода.
По уравнению реакции:
n(NaI) : n(Cl₂) = 2 : 1
У нас даны вещества в отношении
n(NaI) : n(Cl₂) = 0,4 : 0,7 = 2 : 3,5.
Иодид натрия в недостатке, по нему решаем задачу.
По уравнению реакции мольное отношение иодида натрия и йода:
n(NaI) : n(I₂) = 2 : 1 = 0,4 : 0,2.
В результате реакции выделится 0,2 моль йода.
6) Найдем массу выделившегося йода.
M(I₂) = 127 · 2 = 254 г/моль.
m(I₂) = n · M = 0,2 моль · 254 г/моль = 50,8 г.
Масса образовавшегося йода 50,8 г.
#SPJ1
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Обчисли хімічну кількість сульфатної кислоти H2SO4, у якій міститься288,96х1023...
 sokolin210.02.2023 21:06
sokolin210.02.2023 21:06 -
Составь формулу соединения углерода (IV) с серой (II). В формуле на...
 khudobeidiana13.05.2021 03:51
khudobeidiana13.05.2021 03:51 -
7. Какая реакция водной среды жидкого мыла CisH3 COOK? Обоснуйте свой...
 bm2233723.10.2021 12:49
bm2233723.10.2021 12:49 -
Під час розкладання 14, 4 г кальцій карбонату поглинулось 23,4 кДж теплоти....
 maksliifeoy85jo27.05.2020 14:51
maksliifeoy85jo27.05.2020 14:51 -
Можно с дано, решением, формулой.. Какой объем воды образуется для сжигания...
 21Алина11112.05.2020 15:54
21Алина11112.05.2020 15:54 -
1. Закончи уравнения реакций, расставь коэффициенты: а) C+0. - ? + 0...
 умка22211.04.2020 01:12
умка22211.04.2020 01:12 -
Сколько цинка, содержащего 5℅ примесей, требуется для получения 100...
 olchik7504.01.2022 22:15
olchik7504.01.2022 22:15 -
Втехнике карборунл является заненителем алмаза из-за его уникальных...
 HAHAEZ201009.06.2023 22:26
HAHAEZ201009.06.2023 22:26 -
Прошу ,, хотя бы с одной 1)фенол+naoh 2)3-метилвалериановая к-та+метанол...
 iramaun07.03.2022 11:15
iramaun07.03.2022 11:15 -
Приёмы обращения с лабораторным оборудованием, то есть каким должен...
 djkls16.11.2021 01:09
djkls16.11.2021 01:09

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
