Определи, какие из утверждений о кислотах верны. Верных ответов: 3
Если значение рН = 6, то это слабая кислота.
рН кислот варьируются от 0 до 7.
pH уксусной кислоты равно 2,9, а у лимонной
кислоты рН = 2,1. Лимонная кислота является
более слабой.
Желудочный сок содержит соляную кислоту,
которая является очень сильной кислотой.
В кислотной среде бесцветный фенолфталеин приобретает малиновую окраску.
130
363
Ответы на вопрос:
8) 0.77 моль и 7.7 моль 9) 203.4 грамма и 97.2 грамма
Объяснение:
Na2CO3 * 10H2O
Mr = 286 г/моль
m= 220 г
n = 220÷286 = 0.77 моль
n(Na2CO3) = 1× 0.77= 0.77 моль
n(H2O) = x= 7.7 моль
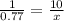
9) Cu(NO3)2 * 5H2O
Mr= 278 г/моль
m= 300 г
n= 300÷ 278 = 1.08 моль
n(CuNO3)2 = 1.08 моль
m(Cu(NO3)2) = 1.08× 188 = 203.04 грамма
n(H2O) = x=5.4 моль
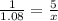
m(H2O) = 5.4×18 = 97.2 грамма
Если будут вопросы, можете отписаться в комментариях.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Определите массу (г) хлорида натрия, полученного при взаимо- действий...
 Sofi20001177726.01.2021 13:03
Sofi20001177726.01.2021 13:03 -
Составьте формулы продуктов реакции, расставьте коэффициенты и составьте...
 Missura200106.10.2020 11:31
Missura200106.10.2020 11:31 -
Осуществить превращения: Ацетилен- бензол- циклогексан...
 rdemchenko08.08.2021 17:48
rdemchenko08.08.2021 17:48 -
Польза и вред синтетических моющих средств...
 Elton1719.08.2021 20:10
Elton1719.08.2021 20:10 -
2. Какую массу тротила (2,4,6-тринитротолуола) можно получить из 112...
 Denaz04.06.2023 02:14
Denaz04.06.2023 02:14 -
Уменя мало времени а делать ! ca+o2⇒ k2o+h2o⇒ p2o5+3h2o⇒ mg+h2so4⇒ ζno+h20⇒...
 Лина199011.02.2021 01:23
Лина199011.02.2021 01:23 -
ОКСИДЫ 1. Допишите уравнения реакций: CuO + HNO3 → BeO + KOH (р-р) →...
 ler2131mold23.05.2021 07:26
ler2131mold23.05.2021 07:26 -
Осуществить превращения. Написать уравнения реакций в молекулярном и...
 Bogdasha30060t07.10.2020 19:01
Bogdasha30060t07.10.2020 19:01 -
В каком виде металлы могут встречаться в природе?...
 keti26128.12.2022 08:49
keti26128.12.2022 08:49 -
Гексан- -(h(2))A+(HOH)- B- Етер | Q- гексахлороциклогексан...
 dimysisdimysis24.10.2022 12:10
dimysisdimysis24.10.2022 12:10

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
