В чем сходство и различие между альдегидами и одноатомными спиртами? С примерами формул, химических реакций
118
286
Ответы на вопрос:
у спиртов есть группа -OH, а у альдегидов -HС=O, кетоны похожи на альдегиды, но у них вместо водорода стоит радикал. Пример. Глюкоза-альдегидоспирт, а фруктоза - кетоноспирт.
C2H5OH - спирт, СH2CHO - уксусный альдегид, CH3COOH - уксусная кислота, CH3-(CO)-CH3 это ацетон
при окислении спирта с OH-группой у последнего углерода образуется альдегид, а при окислении спирта, не у последнего углерода образуется кетон. При дальнейшем окислении альдегида образуется карбоновая кислота
Горение: Как и большинство органических веществ спирты горят с образованием углекислого газа и воды:
C2H5-OH + 3O2 -->2CO2 + 3H2O
При их горении выделяется много теплоты, которую часто используют в лабораториях (лабораторные горелки). Низшие спирты горят почти бесцветным пламенем, а у высших спиртов пламя имеет желтоватый цвет из-за неполного сгорания углерода.
2) Реакция со щелочными металлами
C2H5-OH + 2Na --> 2C2H5-ONa + H2
При этой реакции выделяется водород и образуется алкоголят натрия. Алкоголяты похожи на соли очень слабой кислоты, а также они легко гидролизуются. Алкоголяты крайне неустойчивы и при действии воды - разлагаются на спирт и щелочь. Отсюда следует вывод, что одноатомные спирты не реагируют со щелочами!
3) Реакция с галогеноводородом
C2H5-OH + HBr --> CH3-CH2-Br + H2O
В этой реакции образуется галогеноалкан (бромэтан и вода). Такая химическая реакция спиртов обусловлена не только атомом водорода в гидроксильной группе, но и всей гидроксильной группой! Но эта реакция обратима: для её протекания нужно использовать водоотнимающее средство, например серную кислоту.
4) Внутримолекулярная дегидратация (в присутствии катализатора H2SO4)
В этой реакции при действии концентрированной серной кислоты и при нагревании происходит дегидратация спиртов. В процессе реакции образуется непредельный углеводород и вода. Отщепление атома водорода от спирта может происходить в его же молекуле (то есть происходит перераспределение атомов в молекуле). Эта реакция является межмолекулярной реакцией дегидратации. Например, так:
В процессе реакции происходит образование простого эфира и воды. 5) реакция с карбоновыми кислотами:
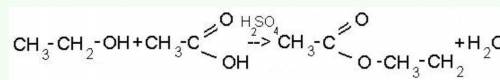
Если добавить к спирту карбоновую кислоту, например уксусную, то произойдёт образование простого эфира. Но сложные эфиры менее устойчивы, чем простые эфиры. Если реакция образования простого эфира почти необратима, то образование сложного эфира - обратимый процесс. Сложные эфиры легко подвергаются гидролизу, распадаясь на спирт и карбоновую кислоту.
6) Окисление спиртов.
Кислородом воздуха при обычной температуре спирты не окисляются, но при нагревании в присутствии катализаторов идёт окисление. Примером может служить оксид меди (CuO), марганцовка (KMnO4), хромовая смесь. При действии окислителей получаются различные продукты и зависят от строения исходного спирта. Так, первичные спирты превращаются в альдегиды (реакция А), вторичные - в кетоны (реакция Б), а третичные спирты устойчивы к действию окислителей.
C2H5-OH + 3O2 -->2CO2 + 3H2O
При их горении выделяется много теплоты, которую часто используют в лабораториях (лабораторные горелки). Низшие спирты горят почти бесцветным пламенем, а у высших спиртов пламя имеет желтоватый цвет из-за неполного сгорания углерода.
2) Реакция со щелочными металлами
C2H5-OH + 2Na --> 2C2H5-ONa + H2
При этой реакции выделяется водород и образуется алкоголят натрия. Алкоголяты похожи на соли очень слабой кислоты, а также они легко гидролизуются. Алкоголяты крайне неустойчивы и при действии воды - разлагаются на спирт и щелочь. Отсюда следует вывод, что одноатомные спирты не реагируют со щелочами!
3) Реакция с галогеноводородом
C2H5-OH + HBr --> CH3-CH2-Br + H2O
В этой реакции образуется галогеноалкан (бромэтан и вода). Такая химическая реакция спиртов обусловлена не только атомом водорода в гидроксильной группе, но и всей гидроксильной группой! Но эта реакция обратима: для её протекания нужно использовать водоотнимающее средство, например серную кислоту.
4) Внутримолекулярная дегидратация (в присутствии катализатора H2SO4)
В этой реакции при действии концентрированной серной кислоты и при нагревании происходит дегидратация спиртов. В процессе реакции образуется непредельный углеводород и вода. Отщепление атома водорода от спирта может происходить в его же молекуле (то есть происходит перераспределение атомов в молекуле). Эта реакция является межмолекулярной реакцией дегидратации. Например, так:
В процессе реакции происходит образование простого эфира и воды. 5) реакция с карбоновыми кислотами:
Если добавить к спирту карбоновую кислоту, например уксусную, то произойдёт образование простого эфира. Но сложные эфиры менее устойчивы, чем простые эфиры. Если реакция образования простого эфира почти необратима, то образование сложного эфира - обратимый процесс. Сложные эфиры легко подвергаются гидролизу, распадаясь на спирт и карбоновую кислоту.
6) Окисление спиртов.
Кислородом воздуха при обычной температуре спирты не окисляются, но при нагревании в присутствии катализаторов идёт окисление. Примером может служить оксид меди (CuO), марганцовка (KMnO4), хромовая смесь. При действии окислителей получаются различные продукты и зависят от строения исходного спирта. Так, первичные спирты превращаются в альдегиды (реакция А), вторичные - в кетоны (реакция Б), а третичные спирты устойчивы к действию окислителей.

Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Решите задачу по химии выведение формул по массовым долям Дано:...
 Настя01011123.08.2020 18:51
Настя01011123.08.2020 18:51 -
ЗА ЛЕГКИЙ ВОПРОС Химические свойства серной кислоты А) взаимодействие...
 LonFostYT01.04.2022 17:39
LonFostYT01.04.2022 17:39 -
Оксидінің жалпы формуласы RO³ болатын элеметтер тобы? А)7А В5а С3а...
 алексей04103.07.2020 23:34
алексей04103.07.2020 23:34 -
Предельные углеводороды. Выполните задания....
 Яна1213318.06.2022 15:58
Яна1213318.06.2022 15:58 -
Обчислити масу водню (H2) кількістю речовини 3 моль...
 KOI22811.09.2022 07:32
KOI22811.09.2022 07:32 -
Определи агрегатное состояние оксида H2O при нормальных условиях....
 Tles10.12.2022 11:44
Tles10.12.2022 11:44 -
Скільки моль кислоти вступить в реакцію з Na, якщо маса солі NaCl=3...
 tayakovalenko24.11.2021 10:44
tayakovalenko24.11.2021 10:44 -
Назовите учёных, работы которых имеют сходство ...
 sashik200522.11.2020 12:49
sashik200522.11.2020 12:49 -
Напишіть рівняння реакцій CaCO+HNO H2S+AL2O3...
 Pomidorka21313.11.2021 04:10
Pomidorka21313.11.2021 04:10 -
Углекислый газ полученный при сжигании анилина массой 18,4 г,пропустили...
 morginen27.04.2022 19:54
morginen27.04.2022 19:54

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
