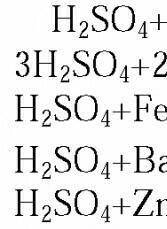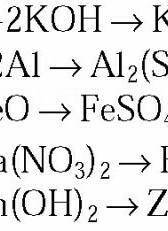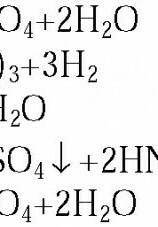Методом электронно-ионного баланса подберите коэффициенты окислительно-восстановительной реакции: 1)K2MnO4+H2O2+H2SO4=MnSO4+O2+K2SO4+H2O
2)K2MnO4+H2O=KMnO4+KOH+MnO2
183
470
Ответы на вопрос:
K2MnO4 + 2 H2SO4 + 2 H2O2 → 2 O2 + MnSO4 + K2SO4 + 4 H2O
Mn⁶ + 4 e- → Mn² (восстановление)
4 O⁻ - 4 e- → 4 O° (окисление)
K2MnO4 является окислителем, H2O2 является восстановителем.
3 K2MnO4 + 2 H2O → 2 KMnO4 + 4 KOH + MnO2
2 Mn⁶- 2 e- → 2 Mn⁷ (окисление)
Mn⁶ + 2 e- → Mn⁴ (восстановление)
K2MnO4 является окислителем и восстановителем (диспропорционирования).
Объяснение:
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Всостав воздуха входит 78% азота. рассчитайте объем и массу (не...
 Markiza1110.08.2020 07:54
Markiza1110.08.2020 07:54 -
Приготовить 7% раствор гидроксида натрия можно смешивая его 3%...
 SkeetNZ28.07.2020 09:30
SkeetNZ28.07.2020 09:30 -
Наибольшее количество атомов содержится в 1 моле : а)сульфата меди(ii)...
 Дако03120404.01.2022 03:44
Дако03120404.01.2022 03:44 -
Расположите следующие Газы H2s,so2,co2,no в порядке возрастания...
 saraavetisyan226.12.2020 07:25
saraavetisyan226.12.2020 07:25 -
, массовая доля в процентах H2CO3, CuO...
 помогите116517.06.2020 11:08
помогите116517.06.2020 11:08 -
. распределить вещества на 2 группы,ТЕСТ НЕ ДЕЛАТЬ, просто поделить...
 Nika09620.06.2021 23:17
Nika09620.06.2021 23:17 -
Яка масова частка CuSO4 в розчині який утворився змішуванням 3,5г...
 natalia2734722.01.2020 05:47
natalia2734722.01.2020 05:47 -
Соотнесите цвет предложенных соединений с их химическими формулами...
 vavilon4ik27.05.2021 08:47
vavilon4ik27.05.2021 08:47 -
Яка кількість теплоти виділяється при повному згорянні 2 кг гексану...
 артём009222.05.2021 19:15
артём009222.05.2021 19:15 -
4.1. Вычислите относительную молекулярную массу СиSO4...
 samira2111101.03.2021 22:59
samira2111101.03.2021 22:59

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.