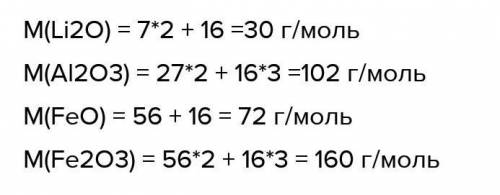Количество вещества. Моль. Число Авогадро. Молярная масса вещества Установи соответствие.
Оксид лития
102 г/моль
Оксид алюминия
160 г/моль
Оксид железа (II)
30 г/моль
Оксид железа (III)
72 г/моль
273
398
Ответы на вопрос:
Объяснение:
M(Li2O) = 7*2 + 16 =30 г/моль
M(Al2O3) = 27*2 + 16*3 =102 г/моль
M(FeO) = 56 + 16 = 72 г/моль
M(Fe2O3) = 56*2 + 16*3 = 160 г/моль
Логика то как раз проста)) пускаю ток и получается вот такая реакция: 3o₂ = 2o₃ и пошла, поехала. из 100 литров кислорода, реагирует 15% т.е. 15л, логично? теперь смотрим. полагая что, объемы измеряются при нормальных условиях составим соотношения объемов кислорода и озона: - это я взял из уравнения реакции, цифры 3 и 2 - это коэффициенты, соотношение объемов, это отношение количеств вещества по уравнению реакции, а это и есть коэффициенты. то есть, смысл коэффициентов - это соотношение количеств веществ нужных для реакции. так вот, объем получаемого озона, равен 2/3 прореагировавшего кислорода: прореагировавший кислород = 15 литров, множим на 2/3 ии: 15*2/3 = ! 10л) ответ: 10 литров озона получится
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Впроцессе na-na+ для перехода атома натрия в и он натрия необходимо...
 Aieks0126.02.2023 02:58
Aieks0126.02.2023 02:58 -
I2+h2so3+h2o=h2so4+hi (i- это йод) напишите степени окисления...
 Kinder164424.11.2021 11:10
Kinder164424.11.2021 11:10 -
Чому в місцях перестановки хімічних елементів у періодичній системі...
 andrey589015.02.2021 02:19
andrey589015.02.2021 02:19 -
Який об єм суміші озону й кисню, де об ємна частка озону становить...
 nasibyannn13.11.2021 18:02
nasibyannn13.11.2021 18:02 -
3. Основным окс ях: а амфотерным - амфотерные гидроксиды. 4....
 nfyrb201430.06.2023 01:14
nfyrb201430.06.2023 01:14 -
Найдите массу соли, образовавшейся при реакции 71 г оксида фосфора...
 gamegame200625.07.2022 08:49
gamegame200625.07.2022 08:49 -
К CuO добавить алюминий...
 НатальяНОВ17.12.2022 11:38
НатальяНОВ17.12.2022 11:38 -
Виконайте завдання та зробіть обчислення ...
 Annakuznetsova200605.01.2021 07:47
Annakuznetsova200605.01.2021 07:47 -
Напишите уравнение реакций для осуществления следующих превращений,...
 CRaBFeed11.12.2021 06:51
CRaBFeed11.12.2021 06:51 -
Наливаємо у пробір- ки по 1 мл розчинів: у першу — купрум(ІІІ)...
 emanuela1603.12.2022 14:37
emanuela1603.12.2022 14:37

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.