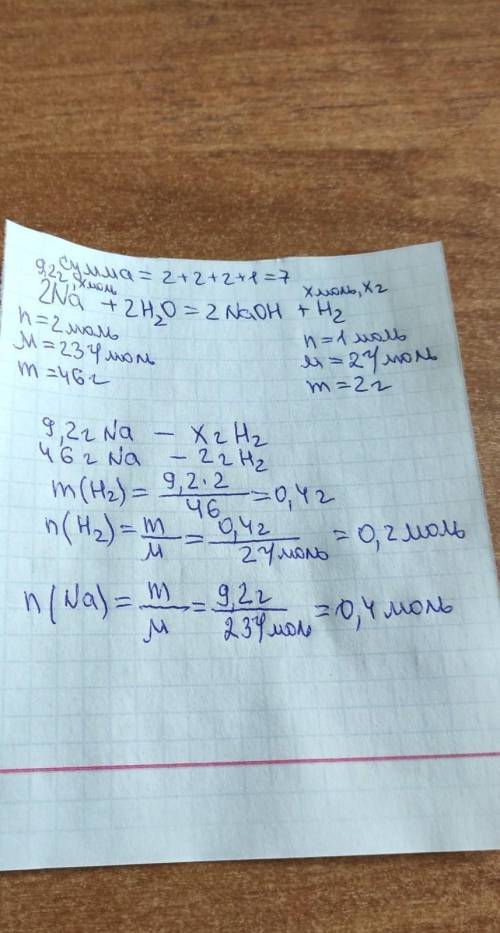9,2 г натрия вступают в реакцию с избытком воды с образованием гидроксида натрия и водорода. Приведена схема, в которой не расставлены коэффициенты. Расставьте коэффициенты в уравнении реакции самостоятельно: Na+H2O=>NaOH+H2
1. Какова сумма коэффициентов в уравнении реакции?
2. Каково количество натрия, вступившего в реакцию (в моль), с точностью до десятых?
3. Каково количество водорода, выделившегося в ходе реакции (в моль), с точностью до десятых?
4. Какова масса водорода (в г), выделившегося в ходе реакции, с округлением до десятых?
157
250
Ответы на вопрос:
Mg(oh)2-гидроксид магнияal(oh)3-гидроксид алюминияcr(oh)3-гидроксид хрома fe(oh)2 и fe(oh)3-гидроксид железаni(oh)2-гидроксид никеляco(oh)2-гидроксид кольбатаmn(oh)2-гидроксид марганцаzn(oh)2-гидроксид цинкаpb(oh)2-гидроксид свинцаsn(oh)2-гидроксид оловаcu(oh)2-гидроксид меди
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Бор диаграммасы бойынша көміртек, азот және оттектің электрондарын энергиялық...
 alinzik321.10.2021 22:19
alinzik321.10.2021 22:19 -
Этиловый спирт не получают из: крахмала глюкозы этана бутана этилена...
 KsyLisa23.01.2020 02:38
KsyLisa23.01.2020 02:38 -
Обчислити массу солі та води 200г розчину з массовою часткою солі 5%...
 cnastya97006.09.2022 05:57
cnastya97006.09.2022 05:57 -
А)-(-с); 9) AvВус; е) (Ал B) » боја и вершин тотаал монтишоого кашки та адал бич...
 Люба01125.03.2020 13:48
Люба01125.03.2020 13:48 -
Написать все органические и неорганические кислоты. поставить волентность на неорганические...
 Barsik1284722.02.2023 13:25
Barsik1284722.02.2023 13:25 -
Органикалык заттардын алынышына виталистердин коз карашы кандай болгон...
 AlexeyB9631.10.2020 14:10
AlexeyB9631.10.2020 14:10 -
A 1. Берілген элемент атомдарының ядро зарядтарын анықтаңдар: хлор, берил- лий,...
 anastasiya205624.09.2021 23:50
anastasiya205624.09.2021 23:50 -
Мемлекеттердің іс - әрекеттерін жікте. Жоңғар хандығы Қазақ хандығы Оқ-дәріні...
 lerabregneva01.11.2022 05:28
lerabregneva01.11.2022 05:28 -
Вкомплексном соединении (nh4)2 [ptcl4] являются ионы...
 дильназ05айдархан01.06.2022 13:42
дильназ05айдархан01.06.2022 13:42 -
С(8)h(18)-октан составить структурную формулу...
 ssssss2213.02.2023 00:38
ssssss2213.02.2023 00:38

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.