химия 8 класс Кусочек цинка массой 13 грамм полностью растворился в растворе серной кислоты. Вычислите массу образовавшейся в данной реакции соли.
Вычислите массу газа, который выделился в результате реакции между металлическим магнием и раствором соляной кислоты массой 127,3г.
Ответы на вопрос:
32,2 г, 39 литров
Объяснение:
1) Запишем уравнение реакции:
Zn + H₂SO₄ = ZnSO₄ + H₂
n(Zn) = n(ZnSO₄) = 13 г / 65 г/моль = 0,2 моль
m(ZnSO₄) = 0,2 моль * 161 г/моль = 32,2 г
2) Запишем уравнение реакции:
Mg + 2HCl = MgCl₂ + H₂
n(HCl) = 127,3 г / 36,5 г/моль ≈ 3,4877 моль
n(H₂) = 1/2 n(HCl) = 1,74385 моль
V(H₂) = 1,74385 моль * 22,4 л/моль ≈ 39 л
Задача №1
Дано:
m(Zn)=13 г
-----
Найти:
m(соли) - ?
Решение
Реакция: 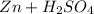 ⇒
⇒ 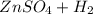 ↑
↑
ν(Zn) = 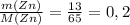 моль (m - масса в (г) [граммы], M - молярная масса, берется из таблицы Менделеева, измеряется в г/моль [грамм поделить на моль] - грамм и грамм сокращаются, остается моль)
моль (m - масса в (г) [граммы], M - молярная масса, берется из таблицы Менделеева, измеряется в г/моль [грамм поделить на моль] - грамм и грамм сокращаются, остается моль)
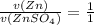 - по уравнению химической реакции (коэффициенты перед веществами в реакции - 1)
- по уравнению химической реакции (коэффициенты перед веществами в реакции - 1)
Тогда:
ν(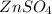 ) = ν(Zn) = 0,2 моль
) = ν(Zn) = 0,2 моль
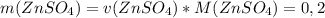 моль
моль 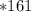 г/моль = 32,2 г
г/моль = 32,2 г
*молярная масса сульфата цинка была посчитана из таблицы Менделеева: M(Zn) + M(S) + 4*M(O) = 65 г/моль + 32 г/моль + 4*16 г/моль = 161 г/моль
ответ: 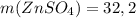 г
г
Задача №2
Дано:
m(HCl) = 127,3 г
-----
Найти:
m(газа) - ?
Решение
Реакция: 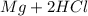 ⇒
⇒ 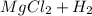 ↑
↑
ν(HCl) = 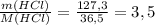 моль
моль
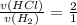 - по уравнению химической реакции (коэффициент перед HCl - 2, перед водородом - 1)
- по уравнению химической реакции (коэффициент перед HCl - 2, перед водородом - 1)
Тогда:
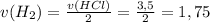 моль
моль
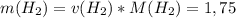 моль
моль 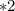 г/моль = 3,5 г
г/моль = 3,5 г
ответ: 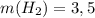 г.
г.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Задание 2. Представьте, что Вы фельдшер или медсест- ра в небольшом...
 lavrovheadshot02.03.2020 11:16
lavrovheadshot02.03.2020 11:16 -
Сколько ячеек было в таблице менделеева?...
 marychevakristi07.07.2021 00:17
marychevakristi07.07.2021 00:17 -
Азотную кислоту нейтрализовали каустической содой. полученный...
 IxJugerNautxl02.05.2023 20:12
IxJugerNautxl02.05.2023 20:12 -
Определите массу порции оксида серы(4), содержащий 7,224*10(в...
 Panikazloy30.06.2021 19:21
Panikazloy30.06.2021 19:21 -
C2h6 - c2h2 - ch3cho - ch3cooh - ch3cooch3...
 Disna200616.01.2022 15:12
Disna200616.01.2022 15:12 -
Какова молярная масса карбоната кальция и сухого остатка образуещегося...
 Vika2004040620.08.2020 20:01
Vika2004040620.08.2020 20:01 -
Со2 + x + na2co3+ y нужно найти что поставить вместо х и у...
 vasiaska23409.03.2022 08:40
vasiaska23409.03.2022 08:40 -
При нагревании бертолетовой соли в отсутствии катализатора ее...
 его1811.06.2021 03:28
его1811.06.2021 03:28 -
Рассчитайте массовую долю(%)атомов фосфора в составе оксида...
 nf78102.12.2022 20:57
nf78102.12.2022 20:57 -
Какую массу поваренной соли требуется добавить к 250 г раствора...
 mashakovalak23413.03.2023 08:16
mashakovalak23413.03.2023 08:16

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
