5. Обратимая реакция выражается уравнением 2SO2 + O2 ↔ 2SO3. В момент равновесия кон¬цент¬рации веществ были: [SO2]=0,02моль/л; [О2]=0,04моль/л; [SO3]=0,03 моль/л. Вычислите значе¬ния константы химического равновесия и исходные концентрации кислорода и оксида серы (IV).
139
269
Ответы на вопрос:
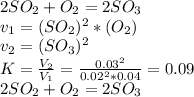
2моль -1 моль-2 моля
расходы : если получено 0,03 моль SO3, для получения такого количество SO3 , в реакции тратится 0,03 моль SO2 и 0,015моль кислорода: 0,03:2=0,015
Объяснение:
Дано массовая доля(углерода)=83,3%=0,833 массовая доля(водорода)=16,7%=0,167 относительная плотность=36 сxhy-? решение: 1.масса(cxhy)=36(плотность по водороду)*2(атомная масса водорода)=72г/моль(масса углеводорода) масса=72г/моль 2.количество углеводорода=1 моль, молекулярная масса=72г/моль 3.находим массу углерода m=0,833*72=60гр 4.находим массу водорода m=0,167*72=12гр 5.находим количество атомов углерода количество вещества=m/m кол-во в-ва=60г/12г.моль=5 моль 6.находим количество атомов водорода кол-во в-ва= 12г/1г.моль=12 моль 7.количественные соотношения сxhy=c5h12 ответ: с5н12 вроде понятно
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Какова его примерная толщина...
 Halimedy09.06.2021 20:46
Halimedy09.06.2021 20:46 -
(Н2S,(BaOH)2 , CaSO4, MgSO4, PbBr2 ,Mg(OH)2 ,NaNO3 ,HF) мына заттардың...
 topghalya22802.03.2020 13:43
topghalya22802.03.2020 13:43 -
Для определения разовой концентрации диоксида азота исследуемый...
 pnasta43419.02.2022 23:31
pnasta43419.02.2022 23:31 -
Суретте күрек тісті белгіленіз...
 natik200513.01.2023 01:10
natik200513.01.2023 01:10 -
Рассчитать потенциал хингидронного электрода, опущенного в буферную...
 GoldenFreddi32208.06.2021 15:33
GoldenFreddi32208.06.2021 15:33 -
При сгорании монохлорпроизводной предельной одноосновной карбоновой...
 sviatolavbazil23.12.2020 04:08
sviatolavbazil23.12.2020 04:08 -
При нагревании парафина он размягчился и переходит в какое состояние?...
 Dosina26.01.2023 20:56
Dosina26.01.2023 20:56 -
Покажи реакцию нейтрализации...
 Королина202231.01.2022 12:20
Королина202231.01.2022 12:20 -
НУЖНО ИЗОБРАЗИТЬ ПОСЛЕДОВАТЕЛЬНОСТЬ Р-ЦИЙ: NО2 - ОЗОН - ВЗАИМОДЕЙСТВИЕ...
 Mishcka1020020.09.2022 10:27
Mishcka1020020.09.2022 10:27 -
Какой объем водорода необходим для полного восстановления марганца...
 gopina04vika18.02.2020 16:27
gopina04vika18.02.2020 16:27

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
