Найти массу сульфата хрома(3) и обьем водорода при н.у , полученных при взаимодействии 5,2г хрома с 98г серной кислотой.
Ответы на вопрос:
Получено 19,6 г сульфата хрома (III) Cr₂(SO₄)₃ и 3,36 л водорода
Объяснение:
Дано: m(Cr) = 5,2 г; m(H₂SO₄) = 98 г.
Найти: m(Cr₂(SO₄)₃); V(H₂).
Решение.
2Cr + 3H₂SO₄ → Cr₂(SO₄)₃ + 3H₂
По уравнению реакции хром и серная кислота реагируют в отношении 2 моль : 3 моль. Найдем количество вещества в заданных массах:
Молярная масса M(Cr) = 52 г/моль
Количество вещества 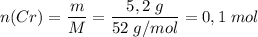 .
.
M(H₂SO₄) = 2 + 32 + 64 = 98 г/моль
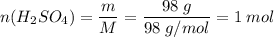
На 0,1 моль Cr требуется 0,15 моль H₂SO₄. Серная кислота дана в избытке. Расчет ведем по хрому.
По уравнению реакции
n(Cr) : n(Cr₂(SO₄)₃) : n(H₂) = 2 : 1 : 3 = 0,1 моль : 0,05 моль : 0,15 моль
Найдем массу образовавшегося сульфата хрома (III) Cr₂(SO₄)₃
M(Cr₂(SO₄)₃) = 2*52 + 32*3 + 16*4*3 = 104 + 96 + 192 = 392 г/моль
m(Cr₂(SO₄)₃) = n*M = 0,05 моль * 392 г/моль = 19,6 г.
Найдем объем выделившегося водорода:
V(H₂) = n*Va = 0,15 моль * 22,4 л/моль = 3,36 л.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Найдите объём(н. число молекул и число атомов каждого элемента 11 мг углекислого...
 Alya1231114.02.2021 00:21
Alya1231114.02.2021 00:21 -
Составьте уравнение реакций между углеродом и следующими а)оксид железа б)оксид...
 Kanat2K406.05.2023 14:41
Kanat2K406.05.2023 14:41 -
Реакции с которых происходят изменения k-koh-k2so4-kcl-kno3...
 SonyaCarrol03.04.2021 14:07
SonyaCarrol03.04.2021 14:07 -
1.какова подаваемого вещества лития прореагирует с водой, если в результате реакции...
 varvara9220.12.2022 23:57
varvara9220.12.2022 23:57 -
Ссоставить формулы веществ,взаимодействующих с разбавленной серной кислотой. naoh=...
 Foxsi200728.12.2020 15:17
Foxsi200728.12.2020 15:17 -
Нужна ! 1. построить 4 возможных изомера вещества c5h11oh. представителем какого...
 2005Человек200513.04.2022 08:34
2005Человек200513.04.2022 08:34 -
Ввашей к уксусной кислоте масса раствора = 150г, с массовой долей кислоты 9% прилили...
 alinakuzmich32416.03.2022 04:10
alinakuzmich32416.03.2022 04:10 -
Визначте молекулярну формулу органічної речовини, якщо при спалюванні 2,45 г цієї...
 myasovkavlad15.05.2021 21:48
myasovkavlad15.05.2021 21:48 -
Вычислить массу цинка и объем кислорода которые необходимы для получения 40,5 грамм...
 Жыж21.12.2020 06:53
Жыж21.12.2020 06:53 -
Вычислить массу алюминия и объем кислорода который необходим для получения 25,5...
 Yanalime200607.11.2021 13:46
Yanalime200607.11.2021 13:46

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.

