Натрий массой 4,6 г полностью растворили в 80мл воды. к полученному раствору прилили 86 мл 20% раствора серной кислоты плотностью 1,14 г/мл. определить массовую долю соли в полученном растворе
130
356
Ответы на вопрос:
w(Na2SO4)=7,79%
Объяснение:
2Na+2H2O=2NaOH+H2↑
n(Na)=m/M=4,6/23=0,2 моль
mp(H2SO4)=86*1,14=98 г
m(H2SO4)=98*0,2=19,6 г
n(H2SO4)=19,6/98=0,2 моль - избыток
2NaOH+H2SO4=Na2SO4+2H2O
n(NaSO4)=0,2*1/2=0,1 моль
m(Na2SO4)=n*M=0,1*142=14,2 г
m(H2)=0,1*2=0,2 г
m(p-p)=4,6+80*1+98-0,2=182,4 г
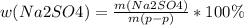
w=14,2/182,4*100=7,79%
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Плотность газообразного органического вещества такая же , как плотность...
 Nina211114.02.2023 13:49
Nina211114.02.2023 13:49 -
Метилэтилкетон изомер альдегид надо...
 vikaMiwka30.05.2022 23:39
vikaMiwka30.05.2022 23:39 -
Составьте молекулярные,полные ионные,сокращенные ионные уравнения:...
 zhigalkinden11.11.2022 08:47
zhigalkinden11.11.2022 08:47 -
Укакого алкина нет изомеров? пентина, этина, пропина, бутина...
 2001snk30.03.2020 22:21
2001snk30.03.2020 22:21 -
Определите степени окисления эл-ов в в-ве: k2so4; al2o3; p2o5; naoh;...
 Itismylife10.04.2021 13:29
Itismylife10.04.2021 13:29 -
Молекулярная формула метанола и этанола,их свойства,применение и...
 Anastasia15Kovaleva14.11.2022 12:33
Anastasia15Kovaleva14.11.2022 12:33 -
2. Распайте с индика тора в трех выданных принумеро- ванных пробирках...
 Dalgat001.11.2020 11:31
Dalgat001.11.2020 11:31 -
10 клас хімія степанова...
 ольга210402.12.2021 15:39
ольга210402.12.2021 15:39 -
3 H2, Mg3P2,2 Al,5 NH3...
 anastasiasestak26.08.2021 05:04
anastasiasestak26.08.2021 05:04 -
Доля металла 5 сульфата двухвалентнного металла равна 40,37 % Найдите...
 1964hade06.09.2022 09:18
1964hade06.09.2022 09:18

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
