При сгорании 20 г органического вещества получили 33,6 л углекислого газа и 18 г воды. Плотность паров вещества по гелию равна 10. Известно, что вещество реагирует с натрием. Формула исходного вещества...; его называют...
213
386
Ответы на вопрос:
Формула исходного вещества 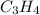 ; его называют пропин
; его называют пропин
Объяснение:
Дано:
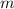 (в-ва)
(в-ва)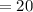 г
г
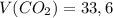 л
л
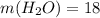 г
г
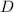 (в-ва/He)
(в-ва/He)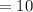
формула вещества-?
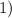 по продуктам сгорания определяем, что в состав искомого вещества входят:
по продуктам сгорания определяем, что в состав искомого вещества входят:
-углерод 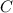 , так как образуется
, так как образуется 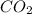
-водород 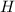 , так как образуется
, так как образуется 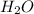
-возможно, кислород 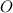 , так как атомы кислорода могли попасть в состав углекислого газа и воды как из простого вещества-кислорода, в котором горело вещества, так и из самого сгоревшего органического вещества
, так как атомы кислорода могли попасть в состав углекислого газа и воды как из простого вещества-кислорода, в котором горело вещества, так и из самого сгоревшего органического вещества
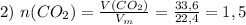 (моль)
(моль)
по схеме 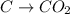
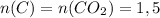 (моль)
(моль)
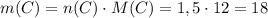 (г)
(г)
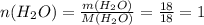 (моль)
(моль)
по схеме 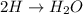
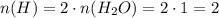 (моль)
(моль)
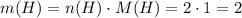 (г)
(г)
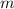 (в-ва)
(в-ва)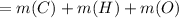
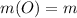 (в-ва)
(в-ва)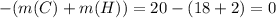
значит, кислород в состав искомого органического вещества не входит
формула вещества в общем виде 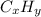
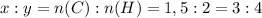
простейшая формула вещества 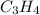
Mпрост = M(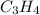 )
)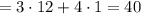 (г/моль)
(г/моль)
Мист = 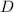 (в-ва/He)
(в-ва/He)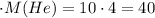 (г/моль)
(г/моль)
k = Mист/Мпрост = 40/40 = 1
значит, истинная формула вещества 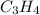 -пропин
-пропин
8na + 10hno3 = 8nano3 + nh4no3 + 3h2o. 8na(0) - 8e = 8na (+1) - окисление восстановитель. n(+5) + 8e = n(-3) - восстановление - окислитель.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Решите что-нибудь, надо, ! сколько грамм сульфата меди потребуется...
 А1А2А3А20.12.2020 13:53
А1А2А3А20.12.2020 13:53 -
35 , : может ли раствор быть одновременно насыщенным и концентрированным?...
 sergejryazanov22816.06.2023 11:31
sergejryazanov22816.06.2023 11:31 -
Кто может внятно объяснить гидролиз? и как писать электрические формулы...
 Электрик201631.05.2022 01:39
Электрик201631.05.2022 01:39 -
Отметьте формулу вещества, с которого можно различить свежеосажденные...
 jhgdfkjg18.03.2021 06:08
jhgdfkjg18.03.2021 06:08 -
Какой объем (н.у.) занимают: а) любой газ количеством 2 моль; б) азот...
 pershikovanata29.04.2021 03:19
pershikovanata29.04.2021 03:19 -
Какое положение молекулярно-кинетической теории подтверждается явлением...
 pushkina8213.07.2020 21:08
pushkina8213.07.2020 21:08 -
реакции ионного обмена» zn(no3)2+ba(on)2= fecl2+lioh= cu(no3)2+k2s=...
 ilonadedyuhinaox7c9l18.05.2020 04:03
ilonadedyuhinaox7c9l18.05.2020 04:03 -
Как изменит окраску лакмус в растворе нитрата аммония? ответ подтвердите,...
 RTAKZM25.05.2020 08:40
RTAKZM25.05.2020 08:40 -
Найдите плотность силона по гелию....
 Ponomorev06.01.2023 07:59
Ponomorev06.01.2023 07:59 -
Вкажіть електроліти під час дисоціації яких у водному розчині утворюються...
 DemonOfFood20.04.2022 21:09
DemonOfFood20.04.2022 21:09

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
