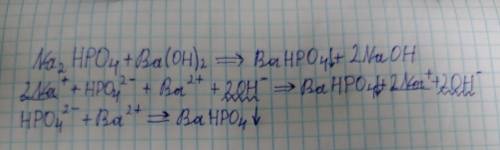Ответы на вопрос:
Объяснение:
Составьте полное и сокращённое ионное уравнение:
Na2HPO4 + Ba(OH)2 →
Объяснение:
Составьте полное и сокращённое ионное уравнение: Na2HPO4 + Ba(OH)2 →
Na2HPO4 + Ba(OH)2 = ВаНРО4 ↓ + 2NaOH
2Na⁺HPO4²⁻ + Ba²⁺ + 2OH⁻ = ВаНРО4↓ + 2Na⁺ + 2OH⁻
HPO4²⁻ + Ba²⁺ = ВаНРО4↓
Kcl = нетр.\лакмус > не изменит цвет kbr = нейтр\ лакмус > не изменит цвет na₂co₃ = щелочная \ лакмус > синий bacl₂ = нейтр. \лакмус > не изменит цвет mgso₄ = кислая\ лакмус > розовый agno₃ =кислая\ лакмус > розовый и так, добавив индикатор, мы сможем точно определить по щелочной среде карбонат натрия (na₂co₃) если прилить его раствор поочередно с пробирками с нейтрально средой, то можно по белому осадку определить хлорид бария (bacl₂ ) bacl₂ + na₂co₃ = baco₃↓ + 2nacl kcl + na₂co₃ ≠ kbr + na₂co₃≠ возьмем растворы с веществами в которых не произошли изменения(kcl и кbr) и добавим в растворы в которых лакмус поменял среду на кислую (предположительно с mgso₄ и agno₃ ). в одной из пробирок увидим, что при добавлении kcl образовался белый осадок, а с kbr - желтый, делаем вывод, что это нитрат серебра (agno₃)/ в другой пробирке - сульфат магния (mgso₄ ) agno₃ + kcl = agcl↓ + kno₃ (белый осадок) тот раствор с нейтральной средой, в котором выпал белый осадок - хлорид калия, желтый - бромид калия agno₃ + kbr = agbr↓ + kno₃ (желтый осадок) итак, все 6 веществ мы определили ионные уравнения не привожу, т.к. много текста.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Решить по ! смесь н-гексана с н-гептаном массой 4.72 грамма была подвергнута...
 sashacom1308.03.2021 18:28
sashacom1308.03.2021 18:28 -
Умоляю ионное и сокращенное ионное уравнения h3po4 + bacl2 = hcl + ba3(po4)2,...
 Disengaliev05.10.2020 14:58
Disengaliev05.10.2020 14:58 -
Написать 5 реакций, при реакции которых образуются соли (с обозначением - в...
 molya9898104.01.2022 07:07
molya9898104.01.2022 07:07 -
Напишите уравнение реакций,соответствующие следующей последовательности превращений...
 SemMandarenova28.02.2022 05:03
SemMandarenova28.02.2022 05:03 -
Как определять атому в уравнениях?...
 Алекс252110.04.2023 06:26
Алекс252110.04.2023 06:26 -
Вчем причина использования переодического закона всеми естественными науками...
 26080709897827.12.2022 10:35
26080709897827.12.2022 10:35 -
Формулой соединения хрома, в которой он проявляет максимальную валентность,...
 zarizatamara0019.05.2020 16:24
zarizatamara0019.05.2020 16:24 -
Какие свойства металлов общие, а какие различные?...
 romanchukana20.07.2021 05:54
romanchukana20.07.2021 05:54 -
Написати реакцію горіння алкана c13h28 + o2 co2 + h2o...
 danyaaseev200613.11.2022 11:13
danyaaseev200613.11.2022 11:13 -
Mgcl2-mgco3-mg(hco3)2-mgco3-co2-n2co3 напишите превращение)!...
 отличник73228.04.2023 10:59
отличник73228.04.2023 10:59

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.