В раствор перекиси водорода массой 150 г опустили небольшое количество катализатора MnO2 . При полном разложении перекиси получили 2 х 10 (-3) м(3) кислорода при 40° и давлении 89 кПа. Вычислите массовую долю (%) перекиси водорода в исходном растворе.
103
363
Ответы на вопрос:
Привет.
2H2O2 --> 2H2O + O2
(MnO2 кат-р)
Оксид марганца в виде катализатора.
Решаем задачу через формулу :
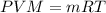
где:
P= давление в кПа
V= объем в Л
M= молярная масса газа
m= масса газа в граммах
R= универсальная газовая постоянная, равная 8.314
T= температура. 273 Кельвина принято считать, как за 0° С, поэтому прибавляем к нему 40°C, и получаем 313° K
89×2×32 = m × 8.314 × 313
Находим значение m:
m= : ≈2.2 граммма.
n(O2) = 2.2/32 = 0.06875 моль
По реакции из 2 моль пероксида водорода образуется 1 моль кислорода
Значит :
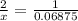
x= 0.1375 моль водорода было в растворе.
m(H2O2) = 0.1375 × 34 = 4.675 грамм.
Находим массовую долю(%)
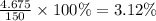
ответ: 3.12%
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Приведите не менее трёх примеров физических тел, которые изготовлены из:...
 Чебурашка123456789023.12.2020 19:21
Чебурашка123456789023.12.2020 19:21 -
Надо формулу вещества...
 мурадаббасов10.01.2023 09:19
мурадаббасов10.01.2023 09:19 -
Задание: Найдите химию в доме Буду безумно благодарен ! Жду ответа...
 Djama123412.02.2020 09:06
Djama123412.02.2020 09:06 -
Реакція нейтралізації H2S+Ca(OH)2...
 сюзи2725.09.2021 00:02
сюзи2725.09.2021 00:02 -
Распишите на ионы соединения: 1) H2SiO3 2) KHSO3 3) MgCO3 4) Ba(OH)2 5)...
 Molderjkee09.03.2021 09:13
Molderjkee09.03.2021 09:13 -
Напишите уравнения реакций, позволяющих осуществить следующие превращения....
 дома914.03.2023 22:58
дома914.03.2023 22:58 -
Осуществите цепочки превращений, составив соответствующие уравнения реакций:...
 OakCadet30.11.2022 13:11
OakCadet30.11.2022 13:11 -
Написать реакцию Окислительно-восстановительную реакцию между кислородом...
 sulfaandrey16.01.2022 12:28
sulfaandrey16.01.2022 12:28 -
Укажіть правильне закінчення твердження: Процес вулканізації каучуку полягає...
 Офелия1234524.04.2022 22:55
Офелия1234524.04.2022 22:55 -
В двух пробирках находятся растворы этилового спирта и уксусной кислоты....
 tanuabekker0022.12.2022 11:50
tanuabekker0022.12.2022 11:50

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
