сгорел углеводород состава 20% Н и 80% С плотность по водороду вещества равна 30. определить формулу сгоревшего вещества.
Ответы на вопрос:
D H2(УВ)=30 - относительная плотность УВ по Н2
D=M(УВ)/M(H2), то
M(УВ)=30*2=60(г/моль)
Пусть формула УВ - СxHy
x:y=(w(C):M(C)):((w(H):M(H))=(80:12):(20:1)=6.666:20=1:3
CH3 - эмпирическая формула
(СH3)*4= C4H12
M(C4H12)=60г/моль
сверяемся с молярной массой, которую нашли изначально - верно
ответ: С4Н12.
P.S. только с 15 получилось
P.P.S. с 30 тоже получилось, просто ответ некрасивый
C4D6
Объяснение:
сгорел углеводород состава 20% Н и 80% С плотность по водороду вещества равна 30. определить формулу сгоревшего вещества.
Пусть формула УВ CxHy, тогда
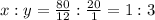
Молярная масса CnH3n
M(CnH3n)=30*2=60г/моль
Откуда
12*n+3*n=60
n=4
C4H12, но такого УВ не существует
Предположим, что в состав УВ входит не протий, а дейтерий
CxDy
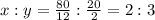
CnH1,5n
12*n+1,5*2*n=60
n=4
C4D6
Mr[CaCO3] = Ar[C] + Ar[Ca] + Ar[O] * 3 = 12 + 40 + 16 * 3 = 100
ω (C) = 12 : 100.0869 * 100 = 12 %
ω (Ca) = 40 : 100 * 100 = 40 %
ω (O) = 48 : 100 * 100 = 48 %
Объяснение:
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
КАКОЙ ОБЪЕМ ГАЗА И МАССА СОЛИ ОБРАЗУЕТСЯ ПРИ ВЗАИМОДЕЙСТВИИ 21.2Г СОДЫ...
 Софяйка23.06.2021 06:59
Софяйка23.06.2021 06:59 -
Определи объём (н. у.) газа, который выделится при действии 200 г 19,6%-ного...
 SureckMozg03.03.2020 07:48
SureckMozg03.03.2020 07:48 -
ПОМАГИТЕ СРОНОО ТЖБ ...
 lyagaeva8714.10.2022 23:27
lyagaeva8714.10.2022 23:27 -
Cu(oh)2-x-cucl2 -cu напишите молекулярные уравнения реакций с которых...
 Tina0517.11.2020 04:11
Tina0517.11.2020 04:11 -
Растворы каких веществ будут проводить электрический ток? а) сульфат железа...
 zb200422.09.2022 07:57
zb200422.09.2022 07:57 -
Який нуклід натріб містить таке ж число нейтронів що й нуклід 24 mg...
 popovamelanaliceysi02.03.2020 13:25
popovamelanaliceysi02.03.2020 13:25 -
В 2 пробирки налейте по 5 6 капель соляной кислоты.В одну пробирку насыпьте...
 Kirill123334114.07.2021 00:20
Kirill123334114.07.2021 00:20 -
И окислительными и восстановительными свойствами могут обладать CO, NaNO3,...
 betmurzaev201528.03.2023 22:42
betmurzaev201528.03.2023 22:42 -
Элемент AZХ испытал два в-распада, сопровождающиеся испусканием двух у-квантов....
 AnastasiaKT26.02.2020 01:57
AnastasiaKT26.02.2020 01:57 -
Выбрать правильный вариант: 1.Які продукти утворилися при розкладанні...
 Urtaol2012.03.2023 04:17
Urtaol2012.03.2023 04:17

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
