3) Написать уравнения реакций взаимодействия метановой кислоты с: - цинком
- оксидом меди (II)
- гидроксидом калия
4) Вычислить массу соли, которая образуется при взаимодействии гидроксида калия с 10% -ным раствором данного соединения массой 20 грамм.
Ответы на вопрос:
Объяснение:
2НСООН + Zn = (НCOO)₂Zn + H₂↑ (на выходе формиат цинка + водород)
2HCOOH+CuO=(HCOO)₂Сu + H₂O (на выходе формиат меди )
НСООН + KOH = HCOOK + H₂O ( на выходе формиат калия)
4.
m(р-ра)=20г
ω(HCOOH)=10%
Определяем массу вещества в растворе:
m(HCOOH)=m(р-ра) * ω(HCOOH) = 20 *0,1 = 2 г.
Определяем молярную массу кислоты и соли:
M(HCOOH) = 1+12+16+16+1 = 46 г/моль
M(HCOOК) = 1+12+16+16+39 = 84 г/моль
Уравнение реакции:
m= 2г.............................Xг
НСООН + KOH = HCOOK + H₂O
M= 46г/моль................84г/моль
имеем пропорцию:
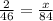
х = 2 * 84 : 46 = 3.65 г.
ответ: 3.65 г соли (формиата калия)
Объяснение:
а) ковалентная неполярная связь
Алмаз представляет собой чрезвычайно твердые, в чистом состоянии бесцветные, абсолютно прозрачные кристаллы, сильно преломляющие свет. Углеродные атомы в кристаллах алмаза связаны ковалентными неполярными связями.
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Определите массу железа необходимого для получения 43.5 г хлорида железа...
 lyudsiya133725.08.2020 20:57
lyudsiya133725.08.2020 20:57 -
Продукты реакции: водород, хлор и гидроксид натрия - образуются при электролизе:...
 Nqva12.01.2021 14:28
Nqva12.01.2021 14:28 -
1) какие степени окисления могут проявлять фосфор и азот в своих соединениях?...
 utyak71709.10.2022 11:03
utyak71709.10.2022 11:03 -
Определить массу и объем углекислого газа, полученного из 200 г известняка,...
 volkego201529.06.2020 12:25
volkego201529.06.2020 12:25 -
Вычислить количество, массу и объем кислорода необходимого для окисления...
 olgakankova8612.10.2021 02:52
olgakankova8612.10.2021 02:52 -
Какой объём воды образуется при сжигании 50 л водорода (н. у.)?...
 Supermegahulk06.03.2020 15:24
Supermegahulk06.03.2020 15:24 -
Задача 1. Сколько граммов гидроксида калия образуется при взаимодействии...
 ЮлияТимофеева09.02.2023 15:12
ЮлияТимофеева09.02.2023 15:12 -
Расставить коэффициенты и указать тип реакции: Fe2O3 + H2--- Fe + H2O; CuCI2...
 кристина215523.05.2020 12:40
кристина215523.05.2020 12:40 -
5 әріптен тұратын химиялық элемент...
 dashutka2003220.05.2022 03:59
dashutka2003220.05.2022 03:59 -
Какова масса 0,45 водорода ...
 Znanija9618.05.2020 05:01
Znanija9618.05.2020 05:01

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
