с решением задачки по химии. Навеску кремниевой кислоты массой 39 г добавили к 200 г 40% раствора едкого натра. Далее к полученному раствору добавили 146 г 30% раствора соляной кислоты. Определите массовую долю хлорида натрия в полученном растворе. ответ приведите в процентах и округлите до десятых.
ответ : 18,6
Ответы на вопрос:
16.9%
Объяснение:
Пишем первую реакцию
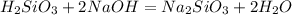
Считаем массу гидроксида натрия
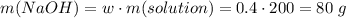
Считаем количество вещества кремниевой кислоты
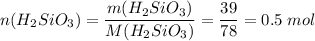
Для реакции нужно вдвое больше гидроксида натрия, т.е. 1 моль или 40 г, а есть 80 г, поэтому расчеты ведем по кремниевой кислоте
Силиката натрия образуется столько же, сколько и было кремниевой кислоты, т.е. 0.5 моль
Пишем вторую реакцию
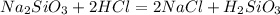
Для полного взаимодействия с 0.5 моль силиката натрия нужно 1 моль кислоты, т.е. 36.5 г. Считаем сколько есть
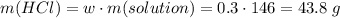
Видим, что соляной кислоты в избытке, поэтому расчеты ведем по силикату натрию
Во время реакции образуется 1 моль хлорида натрия, т.е. 58.5 г и 0.5 моль кремниевой кислоты, т.е. 39 г, которая выпадает в осадок и в массе раствора не считается
Считаем всю массу раствора
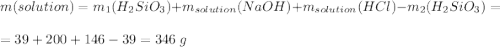
Считаем массовую долю хлорида натрия
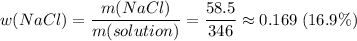
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Где побольше кальция? cao cacl2 (capo4)2 caco3...
 UliaBorodaykevi15.06.2022 19:27
UliaBorodaykevi15.06.2022 19:27 -
Степень окисления оксида хлора который соответствует латинское...
 2004пупик431.10.2022 18:35
2004пупик431.10.2022 18:35 -
Какова масса соли (г), образующейся в результате реакции взаимодействия...
 plidap00rk711.09.2022 04:50
plidap00rk711.09.2022 04:50 -
Сколько кислорода выделиться при разложении 5 моль kclo^3...
 100π10026.10.2021 12:31
100π10026.10.2021 12:31 -
1. дано 10 литров гидроксида натрия. сколько грамм осадка получится...
 Викитирон14.11.2022 11:05
Викитирон14.11.2022 11:05 -
2. сколько литров газа получится, если в реакцию вступит 30мл...
 Mad1nka14.01.2020 18:26
Mad1nka14.01.2020 18:26 -
Железную пластинку массой 5,2 г выдержали в растворе сульфата...
 askardilnaz08.09.2022 13:00
askardilnaz08.09.2022 13:00 -
10 ! формула вещества,с наиболее ярко выраженными кислотными...
 Seks738325.12.2020 23:13
Seks738325.12.2020 23:13 -
Окислительно-восстановительной является реакция разложения: 1)...
 mamanazaruz6019.06.2020 20:36
mamanazaruz6019.06.2020 20:36 -
Втрех пробирках находятся аланин, глицерин и алеиновая кислота...
 maxtigr2414.03.2021 06:31
maxtigr2414.03.2021 06:31

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
