Ответы на вопрос:
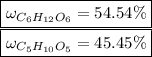
Объяснение:
УравненияСоставим все уравнения реакций:
1) Глюкоза с аммиачным раствором оксида серебра
![C_6H_{12}O_6+2[Ag(NH_3)_2]OH \xrightarrow{t^{\circ }}C_6H_{11}O_6ONH_4+2Ag \downarrow +3NH_3 \uparrow + H_2O](/tpl/images/4867/7838/2c98c.png)
2) Рибоза с аммиачным раствором оксида серебра:![C_5H_{10}O_5+2[Ag(NH_3)_2]OH \xrightarrow{t^{\circ }}C_5H_9O_5ONH_4+2Ag \downarrow + 3NH_3 \uparrow +H_2O](/tpl/images/4867/7838/c5b23.png)
3) Горение глюкозы: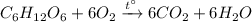
4) Горение рибозы: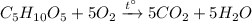
5) Реакция нейтрализации: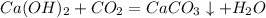
Найдем количество вещества серебра через данное:
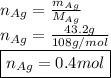
Обозначим количество вещества углеводов через переменные:
Пусть было x моль глюкозы и y моль рибозы
Тогда количество вещества серебра в уравнении 1) равно 2x:
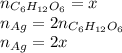
А количество вещества серебра в уравнении 2) равно 2y: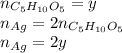
Тогда общее количество вещества серебра равно 2x+2y или 0.4 моль:
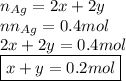
Найдем количество вещества осадка в уравнении 5):
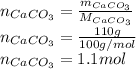
Так как коэффициенты перед углекислым газом и карбонатом равны, то:
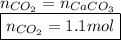
Из уравнения реакции горения глюкозы видно, что количество вещества углекислого газа равно 6x:
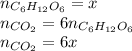
А из уравнения реакции горения рибозы видно, что количество вещества углекислого газа равно 5y:
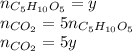
Итого: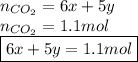
Имеем систему:
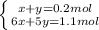
Решая уравнение получим:
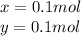
Найдем массу каждого углевода:
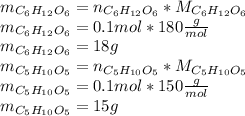
Тогда общая масса равна:
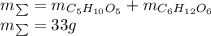
Тогда массовые доли равны:
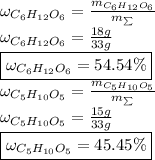
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
1. В 50 мл воды растворили 10г K3PO4. Найти Ткр и Ткип раствора,...
 lenatolkina20.11.2020 04:59
lenatolkina20.11.2020 04:59 -
Причины и последствия процессов, происходящих в неживой природе...
 sanekYakimov25.05.2022 09:10
sanekYakimov25.05.2022 09:10 -
Взрыв пороха физическое или химическое явление?...
 Лизавеликая11111.12.2022 14:06
Лизавеликая11111.12.2022 14:06 -
С чего необходимо измерять объёмы концентрированных кислот и...
 YummyGirl11.05.2021 04:00
YummyGirl11.05.2021 04:00 -
Верны ли суждения о чистых веществах и смесях? 1. Сталь является...
 Nodukam15.04.2020 11:23
Nodukam15.04.2020 11:23 -
Вычисли массу бария, прореагировавшего с 80 г кислорода, если...
 aida280122.03.2023 05:38
aida280122.03.2023 05:38 -
1.Сколько молекул в 40 л смеси, содержащей 20% по объему угарного...
 DamirKa111112.06.2021 04:23
DamirKa111112.06.2021 04:23 -
СРОЧО! В каком количестве молекул угарного газа CO содержится...
 skipos08.04.2023 20:50
skipos08.04.2023 20:50 -
Обчисліть і вкажіть об єм кисню, який витратиться на спалювання...
 cksenia11222.11.2021 21:59
cksenia11222.11.2021 21:59 -
.Установите соответствие между уравнением химической реакции...
 dashapocta07.08.2021 10:34
dashapocta07.08.2021 10:34

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
