Ответы на вопрос:
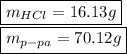
Объяснение:
Алгоритм:Найдем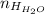 из количества атомов водорода в водеНайдем
из количества атомов водорода в водеНайдем 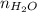 из количества вещества водорода в водеНайдем
из количества вещества водорода в водеНайдем 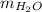 из количества вещества водыВычислим
из количества вещества водыВычислим 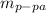 из массы воды и массовой доли HClУзнаем
из массы воды и массовой доли HClУзнаем 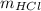 через массу раствора и массовую долю HClРешение:
через массу раствора и массовую долю HClРешение:Найдем количество вещества атомов водорода входящих в состав воды: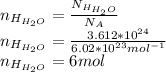
Молекул воды в два раза меньше чем атомов водорода, так как в каждой молекуле воды два атома водорода, следовательно и количество вещества воды в 2 раза меньше:
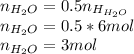
Найдем массу воды в растворе и рассчитаем массу всего раствора на основании массовой доли: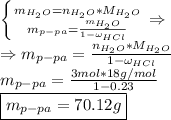
Отсюда же найдем массу безводного хлористого водорода: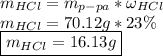
Если в растворе лишь два вещества, то их массовые доли в сумме дают единицу, или 100%: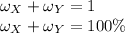
Количества вещества и другие показатели связывают формулы: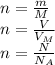
Если в молекуле вещества Y содержится m атомов вещества X, то их количества вещества связаны формулой:
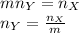
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Напишите уравнение реакций,при еоторых можно осуществить превращения: 1)вычислите...
 Чикчирик1214.12.2021 03:22
Чикчирик1214.12.2021 03:22 -
Из списка элементов составьте формулы оксидов, назовите их li; h(1); cr(5)...
 Hhh234107.04.2023 06:11
Hhh234107.04.2023 06:11 -
Методом электронного подберите коэффициенты, укажите окислитель и восстановитель...
 Overlight133715.06.2020 20:05
Overlight133715.06.2020 20:05 -
Атомную кристаллическую решетку исеет : 1) гидроксид натрия 2) алмаз 3) железо...
 mimimi05513.12.2022 21:15
mimimi05513.12.2022 21:15 -
Какую массу оксида кальция надо взять для получения 148г гидроксида кальция...
 85369219.08.2021 08:43
85369219.08.2021 08:43 -
Напишите уравнения реакций по схеме. назовите вещества c- co2- h2co3- na2co3-...
 amalia20003005.05.2021 18:02
amalia20003005.05.2021 18:02 -
Дописать уравнения реакций, расставить коэфиценты назвать сложные вещества....
 toster133628.04.2020 00:16
toster133628.04.2020 00:16 -
Запишіть рівняння реакції взаємодії олеїнової кислоти з калій гідроксидом....
 bmonolova198017.04.2021 19:43
bmonolova198017.04.2021 19:43 -
Рассчитать объём газа н.у. полученного при взаимодействии na массой 10г с...
 YndoQ02.10.2022 03:05
YndoQ02.10.2022 03:05 -
Составьте формулы солей, образоагных: а) цинком и серной кислотой б) натрием...
 166niko03.03.2021 06:30
166niko03.03.2021 06:30

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
