Ответы на вопрос:
1) Для начала мы запишем схему гальванического элемента:
Pt | Fe⁺³(0,1 моль/л) , Fe⁺²(10⁻² моль/л) || Au⁺(10⁻² моль/л), Au⁺³(0,1 моль/л) | Pt
2) Далее мы определяем какой из них катод и анод, значит из этого гальванического элемента:
Fe - Анод Au - Катод
A⁻ : Pt | Fe⁺³(0,1 моль/л) , Fe⁺²(10⁻² моль/л) || Au⁺(10⁻² моль/л), Au⁺³(0,1 моль/л) | Pt : K⁺
3) Теперь записываем гальванические процессы у катода и анода и потом получим уравнение токообразующей реакции :
K⁺ : Fe⁺² - 1e⁻ → Fe⁺³ | 1 | | 2 | - восстановитель E₁° = -0,77 В
| | 2 | |
A⁻ : Au⁺³ + 2e⁻ → Au⁺ | 2 | | 1 | - окислитель E₂° = 1,40 В
2Fe⁺² - 2e⁻ + Au³⁺ + 2e⁻ → 2Fe⁺³ + Au⁺
2Fe⁺² + Au³⁺ → 2Fe⁺³ + Au⁺ - токообразующая реакция
4) Теперь находим ЭДС у катода и анода по такой формуле:
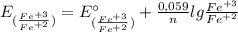
E(Fe⁺³/Fe⁺²) = -0,77 В + 0,059/1 × lg (0,1 моль/л / 10⁻² моль/л) = -0,77 В + 0,059 × lg (0,1 / 0,01) = -0,77 В + 0,059 × lg 10 = -0,77 В + 0,059 × 1 = -0,77 В + 0,059 = -0,711 В
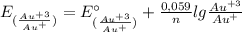
E(Au⁺³/Au⁺) = 1,40 В + 0,059/2 × lg (0,1 моль/л / 10⁻² моль/л) = 1,40 В + 0,0295 × lg (0,1 / 0,01) = 1,40 В + 0,0295 × lg 10 = 1,40 В + 0,0295 × 1 = 1,40 В + 0,0295 = 1,4295 В ≈ 1,43 В
5) Теперь находим ЭДС по полученным значениях :
ε = E(катод) - E(анод) = E(Au⁺³/Au⁺) - E(Fe⁺³/Fe⁺²) = 1,43 В - (-0,711 В) = 1,43 В + 0,711 В = 2,141 В
ответ: ε = 2,141 В
Решено от : 
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Сделайте хотя-бы часть...
 Vika112355678925.11.2022 01:40
Vika112355678925.11.2022 01:40 -
Який обєм кисню і повітря витратиться при згорянні бутану обємом 10 л (н.у.)?...
 apkvava08.08.2022 04:05
apkvava08.08.2022 04:05 -
9. Что такое аллотропия? Приведите примеры простых веществ, являющихся аллотропными...
 34Юлия251125.02.2020 05:31
34Юлия251125.02.2020 05:31 -
7. Начертите в тетради приведенную таблицу. В соответствующих графах запишите...
 lenaglukhova2006.12.2022 00:38
lenaglukhova2006.12.2022 00:38 -
Який об’єм хлору (н.у.) потрібний для повного хлорування метану кількістю...
 Stefan12300515.04.2023 07:19
Stefan12300515.04.2023 07:19 -
А) Зашите угол смежный AOC b) запишите две пары вертикальных углов с)вычислите...
 nikolasosadchey15.06.2023 14:07
nikolasosadchey15.06.2023 14:07 -
З якими речовинами реагуватиме вода : барій , хром , барій оксид , хром (3)...
 yicayejiw29.01.2022 22:24
yicayejiw29.01.2022 22:24 -
5. Составьте формулы высших оксидов и высших гидро- ксидов элементов натрия,...
 SashaZanevskaya24.05.2021 14:15
SashaZanevskaya24.05.2021 14:15 -
Углекислый газ длительное время пропускали через 50 г 0,1%-ного раствора...
 polina135514.01.2021 05:18
polina135514.01.2021 05:18 -
Al→ Al2O3 →AlCl3→Al(OH)3→Al2O3 Вещества назовите. Написать цепочку реакцит...
 on8213.02.2023 04:41
on8213.02.2023 04:41

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
