По закону эквивалентов рассчитайте объем кислорода н.у необходимый для сгорания 70,45 г иттрия.
266
490
Ответы на вопрос:
M(y)=70,45 г z(y)=3 m(eqy)=m(y)/z(y) m(eqy)=88,9/3=29,6 г-экв/моль v₀=22,4 л/моль z(o₂)=2*2=4 v(eqo₂)=v₀/z v(eqo₂)=22,4/4=5,6 л-экв/моль 4y + 3o₂ = 2y₂o₃ m(y)/m(eqy)=v(o₂)/v(eqo₂) v(o₂)=v(eqo₂)m(y)/m(eqy) v(o₂)=5,6*70,45/29,6= 13,33 л
Привет! Сейчас все запишем:
Дано: w₁(H₂SO₄) = 63% , w₂(H₂SO₄)=20%
II. Запишем формулы // Проведем вычисления:
w(E)=m(E)/m(раствора) · 100%
m(E)=w(E)*m(раствора) / 100%
// Пусть мы взяли 100 грамм этого вещества:
m₁(H₂SO₄)=63*100 / 100 = 63 грамма
Теперь сделаем соотношение между массой серной кислоты и новой массой вещества (2):
63 грамма - 20 %
х грамм - 100%
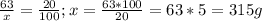
III. Отнимаем от 315 наши 63 грамма кислоты
315 - 63 = 252 грамма воды, при этом в первом растворе было 37 грамм воды (100-63 = 37)
Найдем нужную нам массу воды, которую нужно добавить до 63%-ной серной кислоте, чтобы получить 20%-ный раствор:
252 - 37 = 215 грамм
Готово! Есть вопросы? Напишите, с радостью отвечу на них
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Написать уравнение электричесской диссоциации fecl3...
 Даша010917.09.2020 01:28
Даша010917.09.2020 01:28 -
Очень нужна тем кто Составьте структурные формулы и назовите...
 alinamalinavkjkjh20.10.2020 10:48
alinamalinavkjkjh20.10.2020 10:48 -
Расположите галогенпроизводные в порядке увеличения устойчивости...
 надечка200515.10.2021 12:02
надечка200515.10.2021 12:02 -
Какой объём водорода потребуется для полного гидрирования 2,8...
 kisazaya410.09.2020 12:25
kisazaya410.09.2020 12:25 -
Напишите химическую формулу карбоната магния...
 alexsashinav13.03.2020 19:58
alexsashinav13.03.2020 19:58 -
с химией 1. В какой массе воды необходимо растворить 42 г соли...
 arizonacoins08.02.2021 07:34
arizonacoins08.02.2021 07:34 -
Чему равно зарядовое и массовое число 5 2 he...
 vladchivlad28.02.2020 15:30
vladchivlad28.02.2020 15:30 -
Решите очень номер 435,437 ст. 157; §27 номер 396 ст. 138 §29...
 Лера2206200426.03.2023 17:08
Лера2206200426.03.2023 17:08 -
При взаимодействии 24 г гидроксида кальция с хлоридом аммония...
 husanov18p06h9l01.02.2023 13:12
husanov18p06h9l01.02.2023 13:12 -
Определи массу осадка, который образуется в реакции взаимодействия...
 gvarya0511.12.2020 15:46
gvarya0511.12.2020 15:46

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
