Какая масса и объем хлора затратился на взаимодействие с 5,6г железа, если при этом образовался хлорид железа(|||) ? какая масса продукта образовалась?
144
401
Ответы на вопрос:
Хлорид железа(lll) feci₃ при соединении простых веществ железа и хлора: хлор является сильным окислителем и он от атома железа может максимально отнять три электрона. поэтому степень окисления железа равна +3, а хлора -1 2fe⁰ + 3ci₂⁰ = 2fe⁺³ci₃⁻ (2 моль железа может отдать шесть электронов, 6 атомов хлора могут их принять). при взаимодействии железа с соляной кислотой. ион водорода является не сильным окислителем и ему для восстановления необходим 1 электрон, он может от атома железа отнять его, поскольку железо может отдать 2 электрона, то соединение будет : feci₂ fe⁰ + 2h⁺ci = feci₂ + h₂⁰
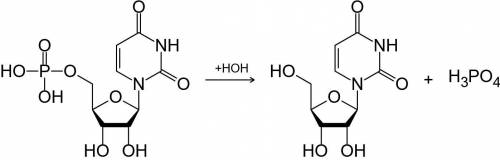
Напишем последовательный гидролиз нуклеотида с названием уридинмонофосфат
1. Гидролиз с отщеплением молекулы фосфорной кислоты с образованием уридина (см. рис. 1)
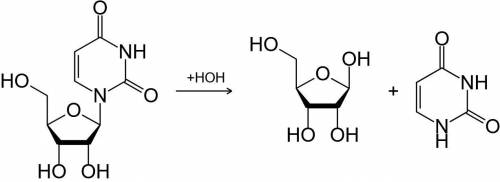
2. Гидролиз с отщеплением рибозы с образованием урацила (см. рис. 2)
Данный нуклеотид может быть в трех вариациях:
- уридинмонофосфат
- уридиндифосфат
- уридинтрифосфат
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Вкаких предложениях речь идет о простом веществе,а в каких о элементе....
 gri6anja2002118.08.2021 18:53
gri6anja2002118.08.2021 18:53 -
Na→na2o→naoh→nacl→na2co3 осуществить превращения...
 flox199809.10.2020 20:49
flox199809.10.2020 20:49 -
Из 34 г нитрата натрия при действии концентрированной серной кислоты...
 крут677603.02.2022 16:38
крут677603.02.2022 16:38 -
Какие из перечисленых явлений относят к ? а)появление приятного...
 daut200101.03.2020 05:51
daut200101.03.2020 05:51 -
Сформулюйте відмінні ознаки хімічної корозії від електрохімічної....
 ирина184407.06.2023 12:42
ирина184407.06.2023 12:42 -
У посудині об ємом 11,2 л міститься водень за н. у. Визначте його...
 optymus13.04.2023 05:01
optymus13.04.2023 05:01 -
Газова суміш складається з азоту масою 42 г та кисню масою 48...
 margaritabennioxwu8x07.06.2020 17:58
margaritabennioxwu8x07.06.2020 17:58 -
хто харашо знает химию виручайте ЗАВДАННЯ: За поданим зразком...
 ЧерриБерри14.05.2023 00:30
ЧерриБерри14.05.2023 00:30 -
Швидко потрібна відповідь!!...
 Apelsin240325.06.2020 01:27
Apelsin240325.06.2020 01:27 -
При жействии на смесь Mg и Cu массой 4 г соляной кислотой (HCl)...
 цццрпппр129.11.2020 00:28
цццрпппр129.11.2020 00:28

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
