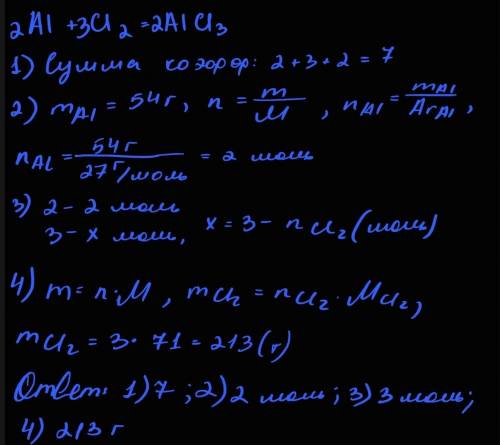Какой объём co2 образуется при действии на 40 грамм известняка содержащего 8% примесей 70гр 15% раствора соляной кислоты. практический выход газа - 80% от теоретического
188
435
Ответы на вопрос:
Caco3 + 2hcl = cacl2 + h2o + co2 n = m/m = v/vм т.к. 8% примесей: m(caco3)ч = 40*0,92 = 36,8 г n(caco3) = 36,8/100 = 0,368 моль т.к. 15%ный р-р: m(hcl)ч = 70*0,15 = 10,5 г n(hcl) = 10,5/36,5 = 0,288 моль по уравнению реакции: n(co2) = 0,288/2 = 0,144 моль считаем по недостатку - кислоте. v(co2) = 0,144*22,4 = 3,23 л v(co2)пр = 3,23*0,8 = 2,58 л
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
На нейтралізацію 300г розчину етанової кислоти витратили калій гідроксид,...
 FenrisYT01.01.2022 23:17
FenrisYT01.01.2022 23:17 -
без якої елементарної частинки неможлива ланцюгова реакція ядерного...
 nikzarubenko27.06.2023 02:28
nikzarubenko27.06.2023 02:28 -
Англійський хімік технолог Генрі Дікон у 1867 році розробив б добування...
 маняня403.10.2020 22:17
маняня403.10.2020 22:17 -
Осущиствите реакции Буду очень благодарен)...
 Kykyshonochek130508.11.2022 22:19
Kykyshonochek130508.11.2022 22:19 -
Подскажите. сколько элементов входит в состав полимера тефлон?...
 6епррг22.09.2020 09:23
6епррг22.09.2020 09:23 -
Как распознать шерстяное волокно и лавсан...
 ksyutitova2017p0bhz401.02.2022 21:09
ksyutitova2017p0bhz401.02.2022 21:09 -
Алкен массой 4,2 г способен присоединить 8 г брома. молекулярная формула...
 01042006кристина010411.02.2022 23:02
01042006кристина010411.02.2022 23:02 -
Чему равно количество вещества кислорода массой 6,4 г...
 cozycoat125.01.2022 20:49
cozycoat125.01.2022 20:49 -
Очень нужно 2 вариант химия...
 Heeellllpppp08.06.2020 22:32
Heeellllpppp08.06.2020 22:32 -
Химия 7 класс Опишіть місце в періодичній системі – це значить : назвати...
 Marfushka7715.10.2022 00:01
Marfushka7715.10.2022 00:01

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.