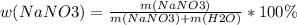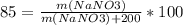Вычислите массу осадка, образующегося при сливании раствора нитрата алюминия и раствора, содержащего 160г гидроксида натрия.
187
454
Ответы на вопрос:
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Формула газа - C3H6 N(молекулы)= 3*10²⁴ M(г/моль) - ? n(моль) - ? m(г) - ? V(л)...
 RAMINA190328.07.2020 23:15
RAMINA190328.07.2020 23:15 -
1. у розчин масою 200 грам , що містив 3 0/0 натрій хлориду, 20% алюміній хлориду...
 jula1985ozpajo22.05.2023 01:01
jula1985ozpajo22.05.2023 01:01 -
По химии составить графическую формулу химических элементов по порядковому номеру...
 геометрия6428.11.2022 02:17
геометрия6428.11.2022 02:17 -
Химия с первого курса технического вуза Задания №2 и №3...
 danila131129.10.2020 21:29
danila131129.10.2020 21:29 -
Как изменяются неметаллические свойства в следующих рядах: А) N → P → As Б)...
 aselb8415.03.2021 21:14
aselb8415.03.2021 21:14 -
Будь ласка 6 завдання до ть...
 fifamobile0106.06.2022 12:41
fifamobile0106.06.2022 12:41 -
Рассчитай численное значение молярной массы водорода. ответ: (2) = г/моль....
 rkarina7909.04.2022 22:28
rkarina7909.04.2022 22:28 -
Как определить объемный состав и среднюю молярную температуру кипения емкости,...
 Lollital16.10.2020 05:15
Lollital16.10.2020 05:15 -
Напишите реакцию разложения щавеливой кислоты....
 angelochekbobi04.07.2021 04:04
angelochekbobi04.07.2021 04:04 -
Суміш масою 50 г, що складається з магній гідроксиду та магній карбонату, прожарили....
 KrasnovaLu8219.01.2020 18:32
KrasnovaLu8219.01.2020 18:32

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.