Вычислите массу соли, которая образуется при взаимодействии 20 процентного раствора уксусной кислоты массой 15 грамм с 10 процентным раствором гидроксида калия массой 22,4г
284
330
Ответы на вопрос:
Чтодано: m(р-раch₃cooh)=15г. ω%(ch₃cooh)=20% m(р-раkoh)=22.4г. ω%(koh)=10% m(ch₃ 1. определим массу уксусной кислоты в 15г. ее раствора с массовой долей 20%: ω%= m(в-ва)÷m(р-ра)×100% отсюда: m(в-ва)=ω%×m(р-ра)÷100% m(ch₃cooh)=ω%(р-раch₃cooh)×m(р-раch₃cooh)÷100%= =20%×15г.÷100%=3г. 2.определим массу гидроксида калия в 22,4г.его раствора с массовой долей 10%: m(koh)=ω%(koh)×m(р-раkoh)÷100%=10%×22,4г.÷100%=2,24г. 3. определим молярную массу уксусной кислоты: m(ch₃cooh)=10+3+16+16+1=46г./моль 4. находим количество вещества уксусной кислоты в 3г.: n=m÷m n(ch₃cooh)=m(ch₃cooh)÷m(ch₃cooh)=3г÷46г./моль=0,07моль 5. определим молярную массу гидроксида калия: m(koh)=39+16+1=56г./моль 6. находим количество вещества гидроксида калия в 2,24г: n(koh)=m(koh)÷m(koh)= 2,24г.÷56г./моль=0,04моль 7. запишем уравнение реакции взаимодействия уксусной кислоты с гидроксидом калия: ch₃cooh + koh= ch₃cook +h₂o 8. анализируем уравнение реакции: по уравнению реакции из 1моль уксусной кислоты взаимодействует 1 моль гидроксида калия. а у нас по условию 0,07моль уксусной кислоты и 0,04моль гидроксида калия, делаем вывод, что уксусная кислота дана в избытке. дальше решаем используя данные гидроксида калия. 9. по уравнению реакции из 1моль гидроксида калия образуется 1 моль уксуснокислого калия, значит из 0,04моль гидроксида калия образуется 0,04 моль уксуснокислого калия. n(ch₃cook)=0.04моль 10. находим молярную массу уксуснокислого калия и его массу количеством вещества 0,04моль: m(ch₃cook)= 12+3+12+16+16+39=98г./моль m(ch₃cook)=n(ch₃cook)×m(ch₃cook)=0,04моль×98г./моль=3,92г. 11. ответ: при взаимодействии 20 процентного раствора уксусной кислоты массой 15 грамм с 10 процентным раствором гидроксида калия массой 22,4г образуется 3,92г.уксуснокислого калия
1,792 л Но так же можно взять 1.8л
Объяснение:
NH4NO3 - НИТРАТ АММОНИЯ
Mr(NH4NO3 ) = 80г/моль
6,4г--х л
80г-- 22,4 л
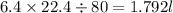
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Назвіть за систематичною номенклатурою вуглеводні...
 2627112307.05.2020 16:28
2627112307.05.2020 16:28 -
Контрольна робота з хімії 7 клас по темі вода. До ть Будь ласка...
 СофияKomarova06.03.2022 00:18
СофияKomarova06.03.2022 00:18 -
Закончить схемы реакций, вставить в пропуски, где это необходимо. 4 примера...
 бог2003109.11.2020 18:20
бог2003109.11.2020 18:20 -
Определите типы реакций в органической химии...
 pochta14736931.03.2023 18:33
pochta14736931.03.2023 18:33 -
6. Задача Ферум (ІІІ) гідроксид кількістю речовини 0,6моль повність розчинили...
 katyaaaasd15.10.2020 17:14
katyaaaasd15.10.2020 17:14 -
«Чи можна довести, що жири містять залишки насичених або ненасичених жирних...
 Yanaaa1316.02.2023 07:33
Yanaaa1316.02.2023 07:33 -
с химией по теме: вычисление массы раствора реагента по количеству продукта...
 LerkaKsuphaMey21.03.2023 12:03
LerkaKsuphaMey21.03.2023 12:03 -
Цис-транс изомеры имеет варианты ответа: 1. ch3–cc–ch3 2. ch3–ch=ccl2 3....
 MAKSON111111919.11.2021 23:18
MAKSON111111919.11.2021 23:18 -
Подберите коэффициенты к уравнениям окислительно-восстановительных реакций...
 funny4303.04.2022 14:20
funny4303.04.2022 14:20 -
Написать уравнения (молекулярные и ионные) взаимодействие гидроксида алюминия...
 missis23ashikhmina23.10.2022 21:02
missis23ashikhmina23.10.2022 21:02

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.
