Достаточно ли 112 литров кислорода для окисления 80кг аммиака? сколько грамм оксида азота при этом может получится?
168
413
Ответы на вопрос:
4nh3 + 5o2 = 4no + 6h2o молекулярный вес аммиака = 14 + 3 = 17 г/моль 80 кг/17г/моль = 4,7 кмоль аммиака взято для реакции. 1 моль любого газа занимает объем 22,4 литра 112 литров кислорода соответствуют 112/22,4 = 5 моль кислорода. 5 моль кислорода способны окислить 4 моль аммиака. у нас аммиака 4,7 кмоль, в 1175 раз больше, следовательно кислорода будет недостаточно. 5 моль кислорода способны окислить 4 моль аммиака с образованием 4 моль оксида азота. молекулярный вес оксида азота равен 14 + 16 = 30 г/моль вес 4 моль оксида азота составит 4 моль * 30 г/моль = 120 г. ответ: 120 г оксида азота no
Реши свою проблему, спроси otvet5GPT
-
Быстро
Мгновенный ответ на твой вопрос -
Точно
Бот обладает знаниями во всех сферах -
Бесплатно
Задай вопрос и получи ответ бесплатно

Популярно: Химия
-
Напишите по три уравнения реакции показывающие свойства щелочей и нерастворимых...
 vgnkrvcv12.08.2022 13:42
vgnkrvcv12.08.2022 13:42 -
Указать вид связи и тип кристалической решетки в n2 ,c2,caf2,of2...
 fykdshklf13.05.2021 19:29
fykdshklf13.05.2021 19:29 -
Дана схема превращений s - so2 - na2so3 - so2 а) составте молекулярные уравнения...
 Lerka0tarelka17.05.2021 19:51
Lerka0tarelka17.05.2021 19:51 -
Вкаждую из трёх пробирок поместили растворы объёмом 1-2 см3: в первую-сульфата...
 Danatil12.11.2022 04:37
Danatil12.11.2022 04:37 -
Из перечня веществ выписать неметаллы: углерод, калий, фосфор водород медь...
 nadezhstepan2010.12.2020 17:50
nadezhstepan2010.12.2020 17:50 -
Каким способом можно проверить соляную кислоту на наличие в ней свободного...
 aigerim34118.12.2022 14:22
aigerim34118.12.2022 14:22 -
1.установите связь между формулой1.установите связь между формулой органического...
 ученик44564312.03.2023 20:00
ученик44564312.03.2023 20:00 -
Какой объем 10% раствора гидроксида натрия (ρ = 1,1 г/мл) может прореагировать...
 малинка18813.01.2022 23:49
малинка18813.01.2022 23:49 -
Al(oh)3+ba(oh)2 молекулярное и ионное уравнение )...
 ildar646421.09.2022 16:16
ildar646421.09.2022 16:16 -
Нужна решить только...
 Filipskaya2013.02.2021 03:44
Filipskaya2013.02.2021 03:44

Есть вопросы?
-
Как otvet5GPT работает?
otvet5GPT использует большую языковую модель вместе с базой данных GPT для обеспечения высококачественных образовательных результатов. otvet5GPT действует как доступный академический ресурс вне класса. -
Сколько это стоит?
Проект находиться на стадии тестирования и все услуги бесплатны. -
Могу ли я использовать otvet5GPT в школе?
Конечно! Нейросеть может помочь вам делать конспекты лекций, придумывать идеи в классе и многое другое! -
В чем отличия от ChatGPT?
otvet5GPT черпает академические источники из собственной базы данных и предназначен специально для студентов. otvet5GPT также адаптируется к вашему стилю письма, предоставляя ряд образовательных инструментов, предназначенных для улучшения обучения.

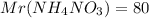 г/моль.
г/моль.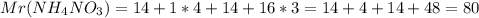 г/моль.
г/моль.